Vaderlandsche letteroefeningen. Jaargang 1868
(1868)– [tijdschrift] Vaderlandsche Letteroefeningen–
[pagina 403]
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Iets over de producten der drooge destillatie van steenkolen.
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
[pagina 404]
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
hetwelk soms groote belemmeringen in het werk gaf. De bereiding der kleuren uit minerale stoffen moest tot opheffing van dit ongemak leiden, van daar het gestadig zoeken naar zulke grondstoffen. Zoo werd het gebruik van Berlijnsch blauw spoedig veelvuldig, en de aanwending van het Schweinfurter-, Zweedsch-, Neuwieder- en Mitisgroen, ondanks hun gevaarlijk karakter als arsenikpraeparaten, als kleurstof voor tapijten, behangsels, gazen, balkleeden, ja, zelfs voor poppengoed niet nagelaten. Geen wonder dus, dat de Anilinkleuren met blijdschap begroet werden; zij toch voldeden aan de meeste vereischten aan eene kleurstof gesteld, ja, overtroffen in vele opzichten de tot nog toe gebruikte. Hare productie, onafhankelijk van toevallige omstandigheden, heeft eene rijke bron van grondstof in de steenkolenteer. Deze is, zooals iedereen weet, een nevenproduct der gasfabrieken, dat in groote hoeveelheden verkregen wordt. Eene beschrijving van de bereiding der Anilinkleuren en haar gebruik in de ververij zal, geloof ik, niemand onwelkom zijn. Hare oorsprong uit de steenkolenteer, een product der drooge destillatie van steenkolen, boezemt mogelijk menigeen belang genoeg in, om nader kennis te maken met de producten dier drooge destillatie. Ik reken het hier noodzakelijk, naar aanleiding van het tweemaal voorkomen der woorden ‘drooge destillatie’, maar vooral met het oog op het opschrift dezer bladzijden, eene nadere omschrijving van het begrip ‘drooge destillatie’ te geven. Het proces der destillatie is iedereen bekend als te zijn: het scheiden van meer vluchtige lichamen van diegene, die in minderen graad die eigenschap bezitten. Diensvolgens scheidt men de vluchtige lichamen door gebruik te maken van hun verschil in kookpunt, b.v. alcohol van water, enz. Er heerscht echter verschil in de beteekenis van dit woord in de scheikunde en in het dagelijksch leven. Het laatste noemt destilleren, overhalen, het scheiden van als zoodanig aanwezige stoffen; de eerste noemt destilleren elk proces, waarbij vluchtige lichamen, onverschillig of zij als zoodanig aanwezig zijn of gedurende de bewerking gevormd worden, overgaan. Men destilleert aether uit alcohol en zwavelzuur; ammoniakgas, welks oplossing in | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
[pagina 405]
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
water ammonia liquida (geest van salammoniak) heet, uit ongebluschte kalk en chloorammonium (salammoniak) enz. Drooge destillatie echter is een woord, dat alleen in de scheikunde gebruikt wordt en welks beteekenis wel eenige toelichting noodig heeft. Het is niet de destillatie van drooge stoffen, want dan zoude de bereiding van ammonia liquida, zoo even genoemd, daartoe behooren. De woordelijke beteekenis helpt dus niet op den weg, maar gaat men het gebruik van het woord na, dan merkt men op, dat alleen de organische scheikunde zich van dit woord bedient; dan blijkt ook, dat het in waarheid een verkolingsproces is bij afsluiting der lucht. Alle organische stof bestaat uit minstens twee, meestal drie, dikwijls vier, zelden vijf of zes bestanddeelen, waarvan koolstof het onmisbaar hoofdelement is: geen organische stof zonder koolstof. Brengt men bij toetreding der lucht genoegzame warmte bij eene organische stof, dan verbrandt zij, dat wil zeggen: de koolstof, waterstof enz. verbindt zich onder vlam- en vuurverschijnsel met de zuurstof der lucht tot koolzuur, water enz. Houdt de verbranding na eenigen tijd op, dan is er meestal kool overgebleven, hetwelk daaruit voortspruit, dat de koolstof in de verbrande stof de overhand heeft, boven de andere bestanddeelen; daarom zullen deze eerder geheel verbrand zijn dan de koolstof, die terugblijft. Is het organische lichaam gasvormig, en eveneens de verhouding der koolstof grooter dan die der andere elementen, dan brandt het met een roet gevende, d.i. koolafzettende vlam. Bij afsluiting der lucht echter, bij afwezigheid van zuurstof, moeten de bestanddeelen der organische stof, als deze verhit wordt, zich met elkander verbinden. Bij drooge destillatie dus, ontstaan verbindingen van koolstof en andere elementen met waterstof en zuurstof, naar verhouding van de samenstelling der stof, en indien deze rijk aan koolstof is, moet kool terug blijven, die geene andere elementen meer vindt om zich er mede te verbinden. Men ziet dus, dat bij verbranding en bij drooge destillatie, het eindresultaat hetzelfde is, n.l. het terugblijven van kool, maar de voorafgegane processen zijn verschillend. Uit het voorgaande blijkt, dat het verkolingsproces bij afsluiting der lucht, slechts toegepast kan worden op die organische | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
[pagina 406]
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
lichamen, die niet vluchtig zijn; de vluchtigen toch zouden destilleeren. De producten, bij de drooge destillatie eener stof ontstaan, zijn verschillend naar gelang dier stof; enkele komen echter bijna altijd voor. Zoo ver heeft de scheikunde het nog niet gebracht, dat zij a priori de producten der drooge destillatie eener stof opgeven kan, meestentijds verkeert zij zelfs a posteriori in het duister omtrent den aard der omzetting. Hoewel het dientengevolge noodeloos schijnt, de oorspronkelijke stof te kennen bij het bestudeeren harer drooge destillatie-producten, is men echter gewoon eerst de oorspronkelijke stof te leeren kennen, en daarna de ontledingsstoffen. Daarom moge ook hier iets over de steenkolen vooraf gaan. De oorsprong dier delfstof wordt algemeen erkend organisch te zijn. Over de vormingswijze van die ontzettende massa brandstof is men het evenwel niet eens. Daaromtrent bestaan verschillende meeningen. Wel komen zij daarin overeen, dat de steenkool ontstaan is uit de ontbinding der planten van het steenkolentijdvak; de plaats van dien plantengroei wordt echter verschillend gesteld; de omstandigheden waarin die ontbinding plaats greep, geeft de een verschillend van den ander op. De meest gehuldigde, tevens de best gegronde meening is de volgende. De moeder der steenkool, was eene landvegetatie, bestaande uit cryptogame vaatplanten, behoorende tot de familiën der Varens (Filices), Zegelboomen (Sigillariae), Paardenstaartachtigen (Equisetaceae) en Wolfsklanwachtigen (Lycopodiaceae). De kruidachtigen onder deze gaven den moerassigen bodem, waarop zij tierden, door de vertakking hunner wortels en bladvormen eenige vastheid, zoodat daarop de boomvarens, zegelboomen en wolfsklauwen (Lepidodendron) groeien konden. De ontbinding dier vegetatie ging steeds voort in het water van het moeras, en op de vergane planten tierde een jonger geslacht. Van tijd tot tijd werd de bodem overstroomd door vloeden, die kiezel, leem en andere stoffen afzetten, welke zich neêrsloegen op de planten en bij het uitdroogen van deze een getrouwen afdruk behielden van hare vormen. Bij het ophoogen van den bodem bleven sommige boomachtige cryptogamen doorgroeien, tot dat hun stam tot op zekere diepte in den grond stak, en dus niet meer om kunnende vallen in dien verticalen stand bedolven geraakte. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
[pagina 407]
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Men meent daarmede de beste verklaring gegeven te hebben voor den loodrechten stand der stammen van varens, sigillariae en lepidodendrons, in verschillende kolenbeddingen gevonden, als hebbende de meeste overeenkomst met wat nog heden ten dage geschiedt b.v. in de moerasbosschen van het oostelijk gedeelte onzer kolonie Suriname, waar zij aan het fransche Cayenne paalt. Het gronddenkbeeld van deze meening is de vorming der steenkool uit de ontbinding onder water eener landvegetatie, meestal in de nabijheid der zee, die van tijd tot tijd door andere stoffen overdekt werd en waarop wederom dezelfde of eene gewijzigde flora ontstond. Eene andere meening omtrent het ontstaan, onderstelt de vorming der meergenoemde delfstof uit eene zeevegetatie overeenkomstig een verschijnsel, dat in ons geologisch tijdperk waargenomen wordt in de Sargasso zee, ten westen der vlaamsche Eilanden, bekend door den schrik, dien het den schepelingen van Columbus inboezemde, meenende, dat zij het einde der wereld bereikt hadden. Zulk eene zeeflora onderstelde men in het steenkolen tijdvak; de in ontbinding verkeerende planten, zouden door leem, kiezel en andere stoffen overdekt zijn geworden. Deze theorie geloofde men beter gegrond dan de eerste met het oog op de chemische eigenschappen van steenkool, bruinkool en turf. De afwezigheid echter van alle zeegewassen in de fossile flora van het steenkolensysteem is de grondigste weerlegging dezer meening. De ontbinding dier plantenmassa's was niet het eenige proces, dat plaats had bij de vorming der steenkool. Terwijl de turfGa naar voetnoot1) door de ontbinding alléén der cryptogame celplanten onder water gevormd wordt, door een langzaam verbrandingsproces alzoo, trad naar alle waarschijnlijkheid bij de steenkolenvorming na | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
[pagina 408]
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
de ontbinding eene andere werking op. Bij de bedekking door leem, klei enz., alzoo bij afsluiting der lucht, moest de verbranding overgaan in eene drooge destillatie, daar alle voorwaarden daartoe aanwezig waren: nl. eene volledige afsluiting der lucht en een tamelijk hooge warmtegraad, die bij drooge destillatie hooger gevorderd wordt dan bij verbranding, zelfs al hebben beide langzaam plaats. Bij dit proces verbond zich een deel der in de planten aanwezige zuurstof met de koolstof tot koolzuur, eveneens een deel der aanwezige waterstof met hetzelfde element tot koolwaterstofverbindingen, voornamelijk tot licht koolwaterstofgas, ook mijn- of moerasgas genaamd en dat bij vermenging met lucht een ontplofbaar mengsel levert, nl. het gevaarlijke schlagende wetter, feu grisou. De vorming der koolwaterstoffen, die de petroleum samenstellen, wordt op dezelfde manier verondersteld. Daar de planten, die eerst aan de ontbinding, daarna aan de drooge destillatie onderworpen waren, tot de koolstofrijke lichamen behoorden, bleef er natuurlijk een koolGa naar voetnoot1) terug, die hoe langer het proces der destillatie geduurd had, des te rijker aan koolstof, te armer aan waterstof, zuurstof en stikstof was. Men begrijpt, dat hier de uitdrukking ‘hoe langer het proces der drooge destillatie geduurd heeft,’ aequivalent is met hoe ouder de steenkolenlagen zijn. En inderdaad vindt men, dat de steenkool uit de oudste lagen rijker aan kool en tevens compacter is dan die uit de jongere, die lichter is en naar verhouding vrij wat meer zuurstof, waterstof en stikstof bevat. In de formatie, voorafgaande aan die van het steenkolentijdvak, vindt men dan ook de anthraciet, en in nog oudere het graphiet, een ijzerhoudende kool. Een overzicht der procentische samenstelling der verschillende koolsoorten moge ter verduidelijking van het voorgaande dienen. Ter vergelijking is die van hout er bij opgenomen. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
[pagina 409]
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Elke soort steenkool bevat, behalve de opgenoemde bestanddeelen, een gehalte aan zwavelijzer, dat voor elk gebruik, dat van die delfstof gemaakt wordt, zeer nadeelig is. Bij het doorzoeken eener kolenbak vindt men allicht in het gruis goudgele kristallen, die regelmatige twaalfvlakken of aanverwante kristalvormen zijn, uit ijzer en zwavel bestaan en ijzerpyriet heeten. Soms vindt | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
[pagina 410]
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
men ook het witte waterkies (straalkies, speerkies), dat eveneens zwavelijzer is. maar in het rhombische stelsel gekristalliseerd. Dat dit gehalte aan zwavelijzer, zooals reeds gezegd is zeer nadeelig voor het gebruik is, zal duidelijk zijn als men bedenkt, dat de metalen, vooral ijzer, spoedig aangetast worden bij het gebruik van zwavelhoudende brandstof en dat, bij de lichtgasfabriekage, het schadelijk zwaveligzuur, zwavelwaterstof en zwavelkoolstof aan dit pyrietgehalte hunne oorsprong verschuldigd zijn. Na dus een woord over de steenkool vooraf te hebben laten gaan, kan nu het onderwerp, waaraan eigenlijk deze bladen gewijd zijn, volgen. Het is mijne bedoeling niet, al de producten der drooge destillatie van steenkolen, wier aantal legio en mogelijk nog niet eens volledig bekend is, hier te behandelen, uit vrees het geduld mijner lezers op een al te zwaren proef te stellen. Slechts die stoffen, die boven de andere in nuttigheid uitmunten en groote waarde voor het dagelijksch leven bezitten, wil ik in hare behandeling en toepassing schetsen. De drooge destillatie der steenkolen geschiedt in het groot uitsluitend in de gasfabrieken. Deze scheiden, op een straks nader te beschrijven manier, de overgegane producten zoodanig als met haar doel overeenkomt, nl. het verschaffen van lichtgas aan hare consumenten. De teruggeblevene coaks, teer en ammoniakaalwater vormen belangrijke nevenproducten, wier waarde den prijs van het lichtgas aanzienlijk verminderen. Het denkbeeld van het gebruiken der gassen van de drooge distillatie dateert reeds uit de vorige eeuw en vond zijne eerste toepassing in de Thermolampen, eene uitvinding van Runkel, door Lebon in 1785 verbeterd. Het was eene inrichting, die tegelijker tijd ter verwarming en ter verlichting diende en waarin het lichtgas uit hout verkregen werd. Deze eerste gasfabrieken in miniatuur vonden weinig toepassing. Eerst in 1810 werd het denkbeeld, lichtgas in het groot te fabriceeren, in Engeland door Mardoch verwezenlijkt. Deze bereidde het uit steenkolen, als eene grondstof, die goedkooper was dan hout. Dit was en is nog de eenige oorzaak, waarom, in landen, arm aan hout, steenkolen boven het eerstgenoemde materiaal verkozen worden, daar toch hout een krachtiger lichtgas verschaft, en bij vrij wat lager temperatuur dan steenkool reeds gas ontwikkelt, zoodat ook minder brandstof vereischt wordt bij de bereiding van gas uit hout. In houtrijke landen is dus dit materiaal te verkiezen boven steenkool. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
[pagina 411]
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
De talrijke producten der drooge distillatie van steenkolen worden verdeeld in: anorganische en organische. De voornaamste der eerste afdeeling zijn: Waterstof, water, kooloxijd, koolzuur, zwavelwaterstof, zwavelig zuur, eenig zwavelkoolstof, stikstof en ammoniak. De organische stoffen overtreffen in getal verre de anorganische en worden verdeeld in: koolwaterstoffen; koolstof, waterstof, zuurstof-; en koolstof, waterstof stikstofverbindingen. Tot de voornaamsten der eerste behoort het moerasgas, zwaar koolwaterstofgas, naphtaline en benzol; der tweede: azijnzuur, phenol en kresol - beiden beter bekend als kreosoot -; der derde: Anilin. Bij de bereiding van lichtgas - waarvan ik nu eenige notatien zal geven - worden de minder vluchtige destillatie producten van de vluchtige door bekoeling afgescheiden, daar zij juist door die mindere vlugheid niet tot de bestanddeelen van het lichtgas kunnen behooren. Die afscheiding geschiedt op de volgende wijze. De steenkolen werden in vuurvaste aarden retorten aan de drooge distillatie onderworpen. Uit elk dier retorten gaat van voren eene buis naar boven, die uitmondt in eene wijdere, gewoonlijk boven de ovens verloopend. In de laatste wordt reeds het aanzienlijkst deel der overgegane min vluchtige stoffen verdicht tot de zoogenoemde steenkolenteer, voor wier geregelde afvoering gezorgd is. De uit deze buis verder strijkende gasvormige lichamen ondergaan eene volkomenere afkoeling in de zoogenoemde verkoelingsbuizen, die in de open lucht staan, 's winters door deze en 's zomers door bevochtiging met water afgekoeld worden, door water met elkander gemeenschap hebben, zoodat het gas, om van de eene buis in de andere te komen door water strijken moet. In dezen toestel verdicht zich teer en water, welk water zich bij het reeds aanwezige voegt en waaraan het gas, bij het doorstrijken, zijn grootste deel ammoniak (koolzure en zwaveligzure ammoniak) afstaat. Deze ammoniakale vloeistof dankt hare bruine kleur en en onaangename reuk aan opgelost teer. De nog in het gas aanwezige ammoniak en teer worden vervolgens door den coakscondensator verwijderd, zijnde eene kast, (in tweeën gedeeld door een tusschenschot, dat bijna op den bodem reikt,) gevuld met coaks, die steeds met water begoten worden. Het ammoniakale water wordt gebruikt ter bereiding van salammoniak en deze gezuiverd door herhaalde omkristallisering. Na deze reinigingen heeft men een gasmengsel, welks bestand- | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
[pagina 412]
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
deelen men gevoegelijk in drie groepen kan verdeelen, naar hunne verhouding bij de verlichting. Deze groepen zijn: 1o de lichtgevende, 2o de verdunnende, 3o de onzuivermakende gassen. De eerste groep bevat de zware koolwaterstoffen van 0.9784 soortelijk gewicht en van 0.832 s.g. De tweede groep bevat: het licht koolwaterstofgas, het waterstofgas en het kooloxijd. De derde groep, die bijna de helft van het mengsel uitmaakt - als ammoniak er bij gerekend wordt - bestaat uit koolzuur, zwavelwaterstof, stikstof en eenig zwavelkoolstof. De gassen der derde groep moeten verwijderd worden, zal het gas bruikbaar zijn. Stikstof en zwavelkoolstof hebben tot nog toe alle pogingen weêrstaan om ze te verwijderen. Het nadeel door hunne aanwezigheid ontstaan is echter niet groot; stikstof en zwavelkoolstof zijn in te geringe hoeveelheid aanwezig, vooral het laatste om het gas onbruikbaar te maken. Maar des te meer is dit het geval met zwavelwaterstof en koolzuur, die beide in groote kwantiteiten tegenwoordig zijn. Zwavelwaterstof toch levert bij zijne verbranding zwaveligzuur - bij het volk bekend onder den naam van zwaveldamp, - hetwelk zeer nadeelig voor de ademhaling is. Dit laatste is ook het geval met koolzuur. Bovendien neemt dit vrij wat hitte weg ter zijner verwarming, en verminderd dus de hitte der vlam. Ter verwijdering van het zwavelwaterstof en koolzuur liet men vroeger algemeen, thans nog op enkele plaatsen, het gas door doelmatig ingerichte kalkbakken stroomen, waarin zich de zwavelwaterstof en het koolzuur met de gebluschte kalk verbonden tot koolzure kalk en zwavelcalcium. De zuivering door kalkhydraat is evenwel niet volkomen, waarschijnlijk voortspruitend uit de omstandigheid dat koolzuur zwavelcalcium eenigzins ontleedt. Daaron heeft men naar andere middelen omgezien ter wegneming van het zwavelwaterstofgas. IJzeroxydhydraat schijnt, blijkens de ervaring, daartoe het beste geschikt en wordt daarvoor bereid naar Laming's methode. Men neemt gelijke deelen gebluschte kalk, zaagsel en sulfas ferrosus (koperood, groene vitriool), mengt de gebluschte kalk met het zaagsel goed door elkander en bevochticht dat mengsel met de opgeloste groene vitriool. De gebluschte kalk werkt zoodanig op het ijzeroxydulzout dat zwavelzure kalk (gips) en ijzeroxydulhydraat gevormd worden. Laat men het mengsel 24 uren aan | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
[pagina 413]
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
de lucht blootgesteld, dan zet zich het ijzeroxydulhydraat in ijzeroxydhydraat om door de zuurstof der lucht. Dit mengsel nu van gips, ijzeroxydhydraat en gebluschte kalkGa naar voetnoot1), Laming's mengsel genoemd, oefent de volgende werking uit op het doorstroomende gas. De nog overgeblevene, niet in gips veranderde ongebluschte kalk neemt koolzuur op, het ijzeroxydhydraat verbindt zich met de zwavelwaterstof tot zwavelijzer. Om het nog overgeblevene koolzuur op te nemen, plaats men voor of achter, liefst achter het Laming's mengsel kalkbakken. Een groot voordeel van dit mengsel is, dat het, na eenmaal gediend te hebben, op eene gemakkelijke en onkostbare wijze weêr tot gebruik geschikt wordt. Spreidt men namelijk het gevormde zwavelijzer aan de lucht uit, dan vormt zich daaruit wederom zwavelzuur ijzeroxydul (groene vitriool). Dit vormt met de aanwezige koolzure kalk, gips en ijzeroxydulhydraat, hetwelk aan de lucht in oxydhydraat verandert. Voegt men daarna weder eenig kalkhydraat bij, dan is het mengsel weder goed. Men kan deze bewerking verscheidene malen herhalen, tot dat de hoeveelheid aanwezige zwavelGa naar voetnoot2) het onbruikbaar doet worden. In plaats van sulfas ferrosus gebruikt men ook een mengsel van ijzerchloruur en mangaanchloruur. Het gasmengsel is na al die bewerkingen genoeg gezuiverd ter verlichting en bevat procentsgewijze de volgen de bestanddeelen waarbij op te merken valt, dat onder zware koolwaterstoffen verstaan moet worden, behalve het zwaar koolwaterstofgas (C4 H4), de aan koolstof rijkere koolwaterstofverbindingen, die, vluchtig zijnde, in geringe hoeveelheid zich in het lichtgas bevinden zooals het benzol (C12 H6) en het acetylen (C4 H2).
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
[pagina 414]
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Ook komen nog voor koolzuur en stikstof, deze zijn hier niet procents gewijze opgegeven. Het gas vermeld onder 1, was bereid uit Wigan Cannel coal, 2 is de analyse van lichtgas uit Heidelberg, 3 de analyse van gas uit Boghead coal, 4 en 5 van Weener lichtgassen. Het zwaar koolwaterstof is het lichtend godeelte van al deze stoffen daar bij hare verbranding kool afgescheiden wordt, die in de vlam gloeiend geworden deze lichtend maakt. Dat werkelijk het zwaar koolwaterstof het lichten der vlam veroorzaakt, blijkt nog duidelijker, als men de verbrandings-verschijnselen der overige bestanddeelen afzonderlijk nagaat. Het moerasgas (licht koolw.) brandt met eene vlam, die niet meer licht verspreidt dan de alcoholvlam; waterstof met eene nauwelijks lichtgevende, kooloxijd met eene weinig lichtgevende vlam. Nu kan men elke weinig lichtende vlam lichtgevend maken door er lichamen in te brengen, die gloeien kunnen, (princiep van Drummonds kalklicht.) Dit beginsel wordt ook op het lichtgas toegepast door de zware koolwaterstoffen te vermeerderen, wat men vroeger deed door het met harsgas te vermengen. Het gas ging dan echter aan een ander euvel mank, nl. dat het niet geschikt was zonder glas gebrand te worden, daar de vlam walmde. Tegenwoordig heeft men het gebruik van harsgas nagelaten en bedient zich van Boghead of Lesmahagokolengas. Het gas wordt, zooals bekend is, door ijzeren buizen den verbruikers toegevoerd en, uit den aard der zaak geschiedt het meten van het geconsumeerde gas ten huize van deze. Het geschied door middel van een werktuig, gasmeter genaamd, hetwelk uit twee hoofdgedeelten bestaat, de maat en de noteertoestel. De eerstgenoemde bestaat uit een blikken cylinder, trommel genaamd, draaiend om eene horizontale as, en door tusschenschotten in vier afdeelingen, kamers, verdeeld, zooals nevensgaande figuur aantoont. Zij is iets meer dan halverwege met water gevuld en de inrichting is zoodanig, dat slechts eene kamer door het in stoomende gas gevuld kan worden, zooals lichtelijk uit de teekening te zien isGa naar voetnoot1). Bij den hier voorgestelden stand der trommel | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
[pagina 415]
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
kan slechts A1 gevuld worden. Het gas in het midden der trommel uit de buis c stroomende drukt tegen den wand e der kamer A1, aan, daardoor draait de trommel in de richting der pijl a b even als de wieken eener windmolen voor de drukking des winds. Het gas vult de kamer tot dat de opening e1 boven het water komt, als wanneer het gas tusschen de trommel en haren mantel uitstroomt. Zoo komen alle kamers aan de beurt en, wanneer zij den stand A4 bereikt hebben, stroomt het gas door de buis f uit. 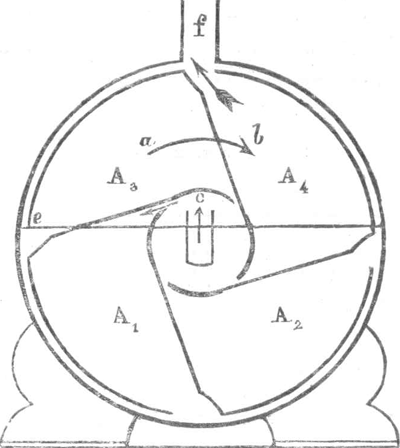 Fig. 1.
De as, waarom de trommel draait, is aan haar einde met eene schroef zonder einde voorzien, die een horizontaal tandrad drijft. Door een eenvoudig zamenstel van raderen wordt deze beweging zoo geregeld, dat eene notering geschiedt van het doorgestroomde gasvolumen. Daartoe is de trommel zoo geconstrueerd, dat het in eene omwenteling doorgestroomde gas een volumen inneemt zoo groot als de ruimte der trommel, die niet met water gevuld is. Eene omwenteling doet dus de wijzers zoo veel gas noteeren als die ruimte bedraagt. Gesteld, die ruimte is 5 kub. voet groot, dan teekent de wijzer na 20 omwentelingen 100 kub. voet gebruikt gas op. Zoo lang nu het water in de juiste hoeveelheid aanwezig is, gaat alles eerlijk in zijn werk; is dit echter niet het geval, dan kan, naarmate er water te veel of te weinig in is, gasverbruiker | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
[pagina 416]
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
of gasleverancier schade lijden. Is er water te veel, dan ook doet de trommel eene omwenteling nadat er zooveel gas doorgestroomd is als de niet met water gevulde ruimte bedraagt, welke nu kleiner is. Dit toepassend op het vorige voorbeeld, zou de wijzer na 20 omwentelingen 100 kub. voet noteren terwijl, iudien de niet met water gevulde ruimte 4 kub. voet groot is, slechts 80 kub. voet door de trommel gestroomd is. Is er te weinig water in de trommel, dan stroomt er meer gas door in eene omwenteling dan genoteerd wordt, wat wel zonder uitlegging begrepen zal worden. Om nu elk het zijne te geven, heeft de gasmeter de volgende inrichting. Voor de trommel bevindt zich een kastje - waarboven de wijzerplaten zijn aangebracht - hetwelk aan zijne boven- en zijwand eene opening heeft door eene schroef gesloten. 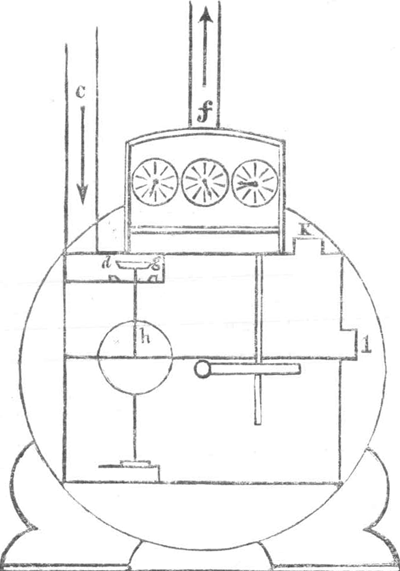 Fig. 2.
Deze schroeven dienen om den waterstand te regelen door nl. bij gesloten hoofdkraan beide schroeven te openen en in k water bij te gieten, tot dat het bij 1 - welke schroef juist ter hoogte | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
[pagina 417]
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
zich bevindt van den normalen waterstand - uitstroomt. Deze vulling behoort wekelijks te geschieden. Bij al te lagen waterstand sluit zich de klep d g door het zakken van den drijvenden kogel h en sluit dus de toegang aan het gas uit de buis c af. Dit zakken der klep veroorzaakt het flikkeren en eindelijk het uitgaan van het licht en is dus eene contrôle van den gasfabrikant op den verbruiker. Bij elken meter is eene opgave van het aantal lichten, dat hij voeden kan. De ervaring heeft geleerd, dat het branden van meer lichten op een meter dan daarop uitgedrukt staat, nadeelig is voor den verbruiker en ook, dat het raadzaam is om, bij eene grootere comsumtie dan 400 kub. voet per uur, deze te meten door middel van twee gasmeters. Het is eene groote onbillijkheid dat de wet geen ijk op de gasmeters vordert, daar het eene waarheid is, dat zij meest allen slecht gecalibreerd zijn. De gasbranders komen in drie soorten voor: 1o. de Argandsche. 2o. de spleet-, 3o. de gaatjesbrander. De twee laatste zijn meer bekend onder den naam van vleermuis of zwaluwstaartbranders en hoewel die naam op beide gemeenschappelijk wordt toegepast, zoo is er nog groot verschil tusschen hen. De Argandbrander, die met een glazen schoorsteen gebruikt wordt, bestaat uit een hollen koperen of porceleinen ring, van boven met gaatjes voorzien, van onderen op eene gaffelvormig vertakte buis staande. De gaatjes, in de bovenste plaat zijn meestal ten getale van 32. Deze branders zijn van allen de beste. Spleetbranders zijn buizen van boven gesloten en dáár alleen van eene fijne spleet voorzien. De vorm van het bovenste gedeelte dier gesloten buis is niet onverschillig voor de deugdelijkheid van den brander; de beste is de elliptisch gewelfde. Ook de vorm der spleet oefent invloed uit; eene diepe spleet, door eene rechte lijn begrensd, is eene nadeelige constructie, omdat daardoor bij de vlam de zijdelingsche punten ontstaan, die onverbrand lichtgas afvoeren. De oorzaak die puntvorming is deze: Het gas ontwijkt door eene diepe spleet in eene bijna horizontale richting daar de brander verticaal staat, maar stijgt door zijn minder soortelijk gewicht dadelijk in de hoogte. De vlam vouwt zich als het ware daardoor toe, en door die verdikking verbrandt het gas minder goed. Dit nadeel wordt bijna geheel opgeheven door de spleet met eene fijne circulairzaag te zagen, zoodat zij begrensd wordt door een cirkel. Zulk eene spleet- | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
[pagina 418]
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
brander levert eene vlam van nagenoeg dezen vorm (nevensgaande figuur). 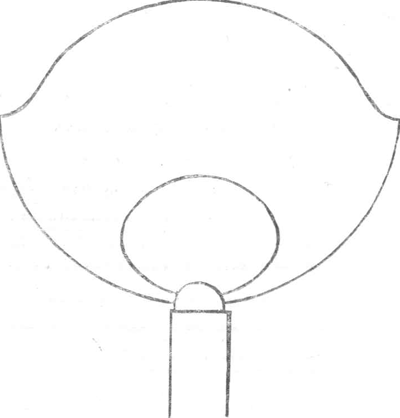 Fig. 3.
In vele opzichten overtreffen de gaatjesbranders de spleetbranders in deugdelijkheid. Deze worden ook gevormd door een aan haar boveneinde gesloten buis, welker bovenwand door twee of drie gaten doorboord is. Hunne vlam lijdt niet aan het euvel der puntvorming. Er zijn eene massa wijzigingen der twee laatste soorten branders voorgeslagen, alle bezuiniging in het gasverbruik beoogende. In plaats van aan die bedoeling te beantwoorden, branden zij blijkens de ervaring veel duurder on voldoet geene vorm beter dan de eenvoudige, hier opgenoemde. Het materiaal waaruit de branders vervaardigd worden was langen tijd koper of staal; doch de verdunning, die het gas onderging door de warmte, die het ontving van den verhitten brander, deed besluiten om minder goede geleiders tot hunne vervaardiging te gebruiken. Tegenwoordig worden zij meest vervaardigd uit speksteen. De consumtie waarvoor zij ingericht zijn is er door ringvormige strepen op aangegeven. Zoo beduidt gewoonlijk een diepe streep 4 kub. voet, elke fijnere 1 kub. voet. Behalve ter verlichting wordt het lichtgas dikwijls aangewend ter verhitting. De opgenoemde branders zijn daartoe niet geschikt. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
[pagina 419]
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
De lichtende vlam geeft niet de grootst mogelijke hitte, daar niet alle aanwezige koolstof verbrandt en de onverbrande, voor hare gloeiing warmte aan de vlam onttrekt. Bovendien zou de lichtende vlam, aangewend ter verwarming, het te verhitten voorwerp met roet bekleeden, wat men liefst vermijdt. Men verandert dus de lichtgevende vlam in eene niet lichtgevende, en bereikt dit doel door toevoeging van lucht. Bunsen heeft dit in zijn gaslamp uitstekend toegepast. In de huishouding gebruikt men eene andere toepassing van hetzelfde beginsel, in de zoogenaamde Elsnersche kooklampen. Bij deze is een stuk metaalgaas boven de uitstroomingsopening gebragt en het gas, dat zich dus met lucht heeft vermengd, wordt boven het gaas ontstoken. De afstand tusschen gaas en uitstroominsopening bepaalt natuurlijk het meerdere of mindere licht der vlam. Men vind licht de gewenschte afstand als men bedenkt, dat het gas, vermengd met 6 maal zijn volumen lucht, geheel zonder lichtverschijnsel verbrandt. Het pijpgas heeft als verlichtingsmiddel in onze dagen een geduchte concurrent gekregen in de petroleum. Bij een onpartijdig oordeel zal men echter aan het eerste de voorkeur moeten schenken, wegens zijne geschiktheid tot verschillende doeleinden, die geene andere vlam bezit. Voor sommige bedrijven toch, is het gas onmisbaar. Den particulieren gebruiker geeft het ontegenzeggelijk veel gemak, en niet het minst te schatten is zijne eigenschap, dat zijne ligtgevende vlam zoo gemakkelijk en doelmatig in een niet lichtende, maar groote hitte gevende, veranderd kon worden. Terwijl tot hiertoe hoofdzakelijk van de gasvormige producten der drooge destillatie van steenkolen sprake is geweest en de gemakkelijk te verdichten ter loop slechts aangeroerd zijn, liggen nu deze laatste aan de beurt. Het is onnoodig op te merken, dat de gasfabrikage het verreweg in belangrijkheid wint van alle andere industrie, die met de producten dier drooge destillatie gedreven wordt. Zijn de andere echter al niet van zoo uitgebreid nut, zij staan toch hoog aangeschreven, en daaronder zeker niet het minst de kleurstoffen, die in pracht de meest geschatte op zij streven of overtreffen. Het gebruik dier kleuren in de ververij dagteekent, zooals reeds in den beginne gezegd is, eerst uit het laatste tiental jaren en nog steeds worden uit dezelfde grondstoffen nieuwe kleuren ontdekt, die even gretig opneming vinden, daar zij of duurzamer | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
[pagina 420]
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
of goedkooper zijn, of beter bij kunstlicht voldoen. Schijnt het al vreemd, dat uit de zwarte steenkool de prachtigste kleurschakeeringen te voorschijn treden, nog wonderlijker klinkt het, dat uit de destillatie-producten dier zelfde stof, zoo onaangenaam riekend, de parfumerie hare geurigste middelen verkrijgt. Hier volgen nu eenige algemeene begrippen omtrent de bereidingswijze dier kleuren waarbij iets van de theorie der ververij gevoegd is. Reeds hier verontschuldig ik mij wegens het voorkomen van chemische formules in den tekst, wat bij dit onderwerp bijna niet te vermijden is, zal het voor den meer of min ingewijde in de chemie verstaanbaar zijn. Men zal er echter slechts zulke aantreffen, die bepaald onmisbaar zijn; wat tot verdere verduidelijking kan dienen zal hier of daar in eene noot bijgevoegd worden. De eerste bewerking, die de steenkolenteer, zooals zij door de gasfabrieken geleverd wordt, ondergaat, is eene destillatie ter scheiding der stoffen lichter en zwaarder dan water. Men noemt deze destillaten lichte en zware steenkolenteer-olie. De lichte gaat het eerst over, bevat dus de vlugtigere bestanddeelen, zijnde hoofdzakelijk koolwaterstoffen, verwant aan het benzol (vlekkenwater). De zware steenkolenteer-olie bevat hoofdzakelijk phenol (kreosoot uit steenkolenteer) en naphtalin, eene koolwaterstofverbinding, die voor korten tijd nog zonder eenige waarde was en waaruit onlangs een prachtige oranjekleurstof bereid is, die reeds in de ververij gebruikt wordt. Wat na deze destillatie terug blijft wordt als teer gebruikt. De bestanddeelen der lichte en zware steenkolenteer-olie ondergaan ter bereiding der kleuren menigvuldige omzettingen, tot wier goed begrip men niet zonder chemische kennis komen kan. Diensvolgens kan hier slechts de bereidingswijze zonder veel verklaring gegeven worden. De Anilinkleuren zullen, als de meest belangrijke, het eerst behandeld worden. Hare grondstof is de lichte steenkolenteer-olie. Men destilleert deze, vangt op wat voor 160o C. overgaat, schudt dit met geconcentreerd zwavelzuur (vitriool) en wascht het met water en koolzure natron (soda). Dit wordt dan aan gefractionneerde destillatie onderworpen, ter scheiding der daarin bevatte koolwaterstoffen. Het eerst overgaande destillaat, kookpunt 80o-100o C. wordt in den handel zeer lichte, wat overgaat bij 100o-120o C. lichte, en wat bij 120o-140o C. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
[pagina 421]
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
overgaat wordt zware benzol genoemd. Deze verschillende destillaten zijn mengsels in verschillende verhoudingen, van drie koolwaterstoffen, waarvan twee voor ons van belang zijn, nl. benzol en toluolGa naar voetnoot1), namen afgeleid van benzoëhars en tolubalsem. In het destillaat dat het eerste overgaat heeft het benzol de overhand, in het tweede en derde het toluol. De scheiding van beiden en de zuivering is een lastige arbeid. In uiterlijk, in oplossingsvermogen en in reuk komen ze veel met elkander overeen, alleen hun smeltpunt is verschillend. Dit is van het benzol hooger dan van het toluol, zelfs zoo, dat het tot scheiding van beide dienen kan. Benzol verstopt soms des winters onbedekte gaspijpen, daar zijne damp, zooals reeds gezegd is, in het lichtgas aanwezig is. De eerstvolgende bewerking dezer destillaten op den weg der Anilinkleurenbereiding is de omzetting van benzol en toluol in Nitrobenzol en NitrotoluolGa naar voetnoot2), stoffen, waarin 1 atoom (= 1 gewichtsdeel) waterstof, door 1 atoom (= 46 gewichtsdeelen) van het lichaam NO4, zijnde eene verbinding van 14 gewichtsdeelen stikstof met 32 gew. deelen zuurstof, en ondersalpeterzuur genaamd, vervangen is. Deze omzetting geschiedt of alleen door salpeterzuur (sterk water) NO5 - eene verbinding, 8 gewichtsdeelen zuurstof meer bevattende dan het lichaam NO4 - of door een mengsel van salpeterzuur en zwavelzuur. - Bij de eerste manier giet men benzol en salpeterzuur, elk afzonderlijk, in cene door koud water afgekoelde spiraalvormige buis, of in goed afgekoelde ijzeren vaten, in de verhouding van 3 deelen salpeterzuur en 2 deelen benzol. Bij deze bereiding geschiedt de omzetting zeer spoedig; veel langer duurt zij bij de tweede manier, n.l. 2 of 3 weken. Bij deze methode brengt men de onder elkander gemengde stoffen in aarden of ijzeren vaten, roert van tijd tot tijd om en bekoelt, zoo noodig. Nadat de omzetting geschied is, scheidt men het nitrobenzol met water af en wascht het daarna met koolzure natron (soda). Om het te zuiveren destilleert men het met waterdamp, bij toevoeging van eenig krijt of soda. Op 6 deelen water gaat 1 deel nitrobenzol over, als men waterdamp van 1 atmospheer drukking gebruikt. Op dezelfde wijze wordt uit Toluol, nitrotoluol verkregen. Nitrobenzol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
[pagina 422]
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
en ook nitrotoluol zijn welriekende stoffen, en het eerste is in de parfumerie als Essence de Mirbane in gebruik gekomen. Uit Nitrobenzol en Nitrotoluol nu, wordt Anilin en Toluidin bereid en wel, door aan deze verbindingen de zuurstof te ontnemen en er waterstof voor in de plaats te brengen. In het algemeen noemt men elk proces, waarbij zuurstof aan eenig lichaam onttrokken wordt, reduceren. Nu is waterstof een der beste reducerende middelen, daar het zich met de zuurstof tot water verbindt. Zoo ook bij Nitrobenzol, volgens de vergelijking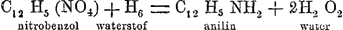 . Door dus waterstof te ontwikkelen in tegenwoordigheid van Nitrobenzol, verkrijgt men anilin en water. Nu kan waterstof volgens verschillende methoden vrij gemaakt worden. De meest gebruikelijke in het onderhavige geval is ijzer met azijnzuur. Men brengt gelijke deelen nitrobenzol, azijnzuur en ijzervijlsel in eene retort en bekoelt, zoo noodig. Nadat de massa bijna vast is geworden, destilleert men ze met kalk in een ijzeren cilinder en verhit ten laatste tot donker gloeihitte. Men zuivert dit destillaat, ruwe anilin geheeten, door nog eens met waterdamp te destilleren. . Door dus waterstof te ontwikkelen in tegenwoordigheid van Nitrobenzol, verkrijgt men anilin en water. Nu kan waterstof volgens verschillende methoden vrij gemaakt worden. De meest gebruikelijke in het onderhavige geval is ijzer met azijnzuur. Men brengt gelijke deelen nitrobenzol, azijnzuur en ijzervijlsel in eene retort en bekoelt, zoo noodig. Nadat de massa bijna vast is geworden, destilleert men ze met kalk in een ijzeren cilinder en verhit ten laatste tot donker gloeihitte. Men zuivert dit destillaat, ruwe anilin geheeten, door nog eens met waterdamp te destilleren.
In het bovenstaande is steeds gelijktijdig sprake geweest van benzol en toluol en van de daaruit op gelijke wijze bereide stoffen. Dit is daarom geschiedt, omdat Hoffmann heeft aangetoond, dat de meest bekende anilinkleurstof, het anilinrood, als voorwaarde van vorming, beiden vereischt, wat waarschijnlijk ook wel bij de andere kleuren het geval zal zijn, daar zij tot dusverre nog allen uit toluidinhoudend anilin bereid zijn geworworden. Bovendien geloof ik niet, dat de duidelijkheid benaddle wordt door het gelijktijdig noemen dier beide stoffen, aangezien hare analoge verhouding geene verwaaring in het begrip der omzetting geven kan. Het anilin en toluidin zijn bases, dat wil zeggen, stoffen, die zich met zuren, b.v. zwavelzuur, salpeterzuur, zoutzuur, (geest van zout) arsenigzuur, (rattekruid) enz. tot zouten kunnen verbinden. Uit de zouten van het anilin en uit het anilin zelf worden, door de inwerking van verschillende stoffen, de anilinkleuren bereid. Het is onmogelijk hier een denkbeeld te geven van de samenstelling der anilinkleuren, daar ik alsdan bij mijne lezers meer chemische kennis moet veronderstellen, dan billijkerwijze verwacht mag worden. Den weetgierigen lezer, genoegzaam daarvan | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
[pagina 423]
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
voorzien, verwijs ik, indien hij meer wil vernemen omtrent de constitutie der anilinkleuren, naar Kekulés Organische Chemie 2ter Band, S. 668 u. folg. of van denzelfden schrijver, Chemie der Benzolderivate, over dezelfde zaak. Voor dat de bereidingswijze der verschillende anilin- en andere kleuren uit de producten der drooge destillatie van steenkolen volgt, meen ik, niet ondienstig, iets over de theorie der ververij vooraf te laten gaan, opdat bij de bereidingswijze tegelijkertijd de toepassing dier kleuren in de ververij gegeven kan worden. De stoffen, die aan de bewerking van het verwen onderworpen worden, zijn van plantaardigen of dierlijken oorsprong en naar dien oorsprong verschillend samengesteld. Zij ondergaan, voordat dat zij geverfd worden, verschillende voorbereidende bewerkingen, die allen ten doel hebben de deugdelijkheid en zachtheid van het weefsel te bevorderen, de holheid tegen te gaan en niet het minste - het goed gelukken van verven of drukken. Vlas en hennip worden daartoe geroot, om de vezels van de harsachtige deelen te ontdoen, die het weefsel, als zij niet goed verwijderd zijn, hol maken. Dan volgt na nog eenige bewerkingen het bleeken, hetwelk een omhulsel der vezel moet vernietigen, dat het opnemen der kleurstof tegenhoudt. Wol ondergaat eene zuivering van het smeer, dat zij bevat, hetwelk bij de fijnere wolsoorten meer bedraagt dan bij de gemeenere. - De zijde wordt gekookt met zeep om het hol worden van het weefsel te voorkomen en daarna nog met soda. De vezel, die al de voorafgaande bewerkingen heeft ondergaan is geschikt de kleurstof in zich op te nemen. Deze opneming geschiedt direct of door tusschenkomst van eenig ligchaam, bijtmiddel (mordant) geheeten. Het is nl. noodig, zal de kleur blijvend zijn, dat de kleurstof, in de vezel opgenomen, daarin in eene vaste vorm zich bevinde. Evenwel is hierbij op te merken, dat onopgeloste of onoplosbare kleurstoffen geene kleurende werking uitoefenen (met uitzondering van ijzerroest). Wanneer de kleurstof niet uit zich zelve in de vezel den vasten toestand aanneemt, dan brengt men in deze zoodanige stof, die met de kleurstof eene onoplosbare verbinding vormt. Zulk een lichaam noemt men bijtmiddel (mordant). Men heeft bijtmiddelen, die de kleur dezelfde laten en ook, die ze veranderen; men gebruikt ze naar behoefte. De niet gekleurde zijn: aluin, azijnzure aluinaarde | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
[pagina 424]
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
tinchloruur (tinzout). De gekleurde zijn azijnzuur ijzeroxyd, zwavelzuur ijzeroxydul (groene vitriool), koperzouten en looizuur. Omtrent den aard der werking, die bij het verven optreedt, verkeert men nog in het onzekere. Vroeger hield men het er algemeen voor en thans nog verscheidenen, dat het verven eene uiting is van chemische verwantschap tusschen vezel en kleurstof en bij gebruik van een mordant, tusschen deze drie. Tegenwoordig is de mechanische theorie de meest gehuldigde, die het kleuren in eene adhaesie tusschen kleurstof en vezel veronderstelt. Tot steun der chemische theorie voert men aan de ontleding van zouten door het weefsel, bovendien dat de neergeslagen kleurstof verschilt naar den aard van de te kleuren vezel. De mechanische theorie heeft veel meer gronden voor zich. Men stelt zich de werking der adhaesie tusschen de kleurstof en de vezel voor, zooals die plaats grijpt tusschen kool en kleurstof. Zij voert tegen de chemische theorie aan dat de vezel vóór hare kleuring zoowel als na hare ontkleuring dezelfde structuur vertoont, bovendien, dat de plantaardige en de dierlijke vezel dezelfe verhouding toont tegenover kleurstof, wat niet plaats zou grijpen als de kleuring eene chemische werking was, daar die vezels zeer in samenstelling verschillen. Nu overgaande tot de bereidingswijze der Anilinkleuren, moet opgemerkt worden, dat onder haar eene den boventoon voert als zijnde verreweg de belangrijkste, ook als uitgangspunt voor andere kleuren. Hoewel zij in ancienniteit - om dit woord hier te gebruiken - wijken moet voor eene harer zusters, zal zij echter om de zoo even genoemde eigenschap het eerst behandeld werden. De kleur, waarvan hier sprake is, is het Anilinrood dat behalve dezen naam nog verscheidene andere bezit b.v. fuchsin - van de fuchsia - Magenta, Solferino enz. Het werd het eerst ontdekt door Hofmann in 1857. Zijne bereidingswijze was echter voor de praktijk niet aanbevelenswaardig. De methode, door Verguin van Lyon eenigen tijd later gevonden, was beter daartoe geschikt en in 1859 nam de bekende firma Renard frères et Franc patent daarop. Deze bereiden het fuchsin door 10 deelen anilinolie - zoo wordt toluidin houdende anilin genoemd - met 6 of 7 deelen watervrij tinchlorid gedurende 15-20 minuten te koken. Eerst wordt het mengsel geel, dan roodachtig, eindelijk fraai rood, in dikke lagen schijnt het zwart. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
[pagina 425]
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Behalve deze methode bevatte hun patent nog menige andere bereidingswijze. Van de vele voorgeslagene en in praktijk gebrachte methoden, haal ik hier slechts aan die van Schlumberger, die in plaats van tinchlorid salpeterzuur kwikoxydul gebruikt. Zij heeft wel voor boven die met tinchlorid. Eene andere weder is die van Depouilly et Lauth, uit Anilinolie en salpeterzuur Anilin; nog eene andere, die van Gerber-Keller uit Anilinolie en salpeterzuur kwikoxyd. De twee laatstgenoemde firma's hadden wegens haar patent een langdurig proces met de houders van het eerste patent Renard frères et Franc, dat ten gunste dezer laatsten beslist werd door de onderzoekingen van Prof. A.W. Hofmann, die aantoonde, dat de kleurstof door de beide eerste firma's vervaardigd, verbindingen van hetzelfde lichaam zijn als de kleurstof der firma Renard frères et Franc, zoodat deze het monopolie der Anilinroodbereiding in Frankrijk verkreeg. Van hoeveel gewicht die uitspraak voor de betrokken partijen was, kan men daaruit opmaken, dat de meergemelde firma Renard et Franc binnen korten tijd millioenen met haar fabriekaat verdiende, en dat later de firma overging in eene naainlooze vennootschap, met een kapitaal van vier millioen francs. Tegenwoordig wordt het meeste Anilinrood met arsenikznur bereid. Medlock, een engelsch chemicus, nam daarop patent 18 Jan. 1860 en Nicholson 26 Jan. 1860. Het ongezuiverde Anilinrood is een zwartroode massa met een groene metaalglans en eene schilferige breuk. Het wordt gezuiverd door gebruik te maken van zijne mindere oplosbaarheid in zoutoplossingen dan in water, en komt in handel voor als kristallen of als oplossing. Om er mede te verven lost men de kristallen in kokend water op, schuimt de oplossing, filtreert ze door vilten zakken en verft direct met het filtraat zijde en wol, in de nuances genaamd: Rose des Alpes, Anilinrosa, Carmoisine, Magenta enz. Katoen vordert bijtmiddelen, zooals een bad van olyvenolie, eenig zwavelzuur en alcohol, en water; of looistoffen, of natronaluminaat. Er komt meestal slechts ééne nuance van de roode kleur bij het katoenverven voor. Op het anilinrood laat ik de vroegst bekende anilinkleur volgen. Zij draagt den naam van Anilinviolet, maar is evenmin als het anilinrood van andere namen misdeeld. Eenigen dezer | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
[pagina 426]
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
zijn: Mauve, Dahliablauw, Tyrisch purper, Violet Parme enz. W.H. Perkin, de ontdekker dezer kleur, nam den 26. Aug. 1856 patent op de volgende bereidingswijze. Hij vermengde de oplossingen van aequivalente hoeveelheden van zwavelzuur anilin en zure chroomzure kali en verkreeg een zwart neerslag hetwelk na zuivering Mauve gaf. Ook van deze kleurstof bestaan verschillende bereidingswijzen. Depouilly en Lauth namen in Frankrijk (1860) patent voor de volgende methode. Een anilinzout wordt met eene oplossing van chloorkalk zoolang behandeld, totdat er een donker violette neerslag komt. Deze wordt vervolgens gezuiverd. Al de voorgeslagene methoden zijn weinig productief daar de opbrengst slechts 5-10% van het gebruikte anilinzout is. Dit maakt Perkin's Violet zeer duur. Men zon er dus op eene goedkoopere violette kleur te vervaardigen. Het gelukte inderdaad het anilinrood in de kuip in violet te veranderen, door middel van een mengsel violet mordant genaamd. Deze methode heeft echter haar belang verloren door de ontdekking van Girard, die violet uit Anilinrood bereidt door het 5-6 uren lang met zijn gelijk gewicht Anilin te verhitten op 165o-180o C.A.W. Hofmann verkreeg het prachtige Dahlia-violet door anilinrood met Jodaethijl te behandelen. Deze kleur is zeer kostbaar om het dure materiaal Jodaethijl, en wordt slechts gebezigd om zijde te verven. Men had tot voor korten tijd groote last bij het gebruik der Anilinkleuren van hare onoplosbaarheid in water en moest zich van de dure alcohol bedienen, welke bovendien nog dit ongemak opleverde, dat, door het spoedig verdampen van dit oplossingsmiddel, de kleurstof zich ongelijk verdeelde over het weefsel. Aan Gaultier de Claubry heeft de industrie de gewichtige ontdekking te danken, dat de in water onoplosbare Anilinkleuren - in water oplosbaar zijn alleen fuchsin, Perkin's violet en bleu soluble - door ze met plantenslijm, gomoplossingen, eene oplossing van amandeloliezeep, dextrin, stijfsel, Glycerin of dierlijke lijm te behandelen, in water oplosbaar worden. Het beste voldoet een aftreksel van den Panama-bast (Quillaïa saponaria) en van het Egyptische zeephout (Gypsophila strutium). Met deze oplossingen verft men wol en katoen met een bijtmiddel en wel voor katoen hetzelfde als bij het fuensin, voor wol een bijtmiddel uit tinchorid, aluin en wijnsteen bestaande. De zijde heeft geen bijtmiddel noodig. De nuances worden | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
[pagina 427]
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
langs verschillende wegen verkregen: of door verandering van de temperatuur van het bad of door het bezigen van verschillend violet. De nuances heeten: Anilinlila, Dahlia, Violenblauw, Hijacinth, echt Eminence, Amethyst enz. Op dezelfde wijze als C.A. Girard zijn violet verkreeg door fuchsin met anilin té verhitten verkreeg hij bij toevoeging van meer anilin, eene blauwe kleurstof bleu de Paris, blen de Lyon genaamd. Price bracht eene wezenlijke verbetering aan de methode door zijne waarneming, dat een organisch zuur de bewerking bespoedigt. Volgens Prof. P. Bolley, verkrijgt men eene voordeelige productie door het gebruik van benzoëzuur. Nog twee methoden noem ik bier; de eene waarop O. Sacks in Londen patent heeft genomen. Bij deze smelt men 2 deelen anilinrood met 8 deelen anilinolie en lost daarin ½ deel gewone zeep op. Dit mengsel wordt 2 uren tot 210o-220o C. verhit. Daarna wordt het gezuiverd. De andere is de methode van Schäffer en Gros-Renaud door fuchsin en eene alcalische oplossing van gomlak voortdurend te koken, waardoor eene prachtig blauwe kleur ontstaat. (Bleu de Mulhouse). Nog komen voor het bij kunstlicht kleur houdende bleu de lumière en het door zwavelzuur oplosbaar gemaakte bleu soluble. Het verven van wol met Anilinblauw gaat, even als bij het violet, door middel van een ordant; katoen heeft dezelfde bijtmiddelen voor deze kleur noodig als bij het violet en rood, maar neemt het blauw zoo goed niet aan. Zijde behoeft geen bijtmiddel. Anilingroen, ook aldehyd groen genoemd - naar zijne bereidingswijze - werd door C.J. Eusèbe in 1864 te Parijs ontdekt. Men lost ter zijner bereiding fuchsin in tamelijk sterk zwavelzuur op en voegt er aldehyd bij, verhit in een zandbad, totdat een droppel van het mengsel, in zuur gemaakt water gebracht, eene groene kleur aanneemt. Dan voegt men er kokend water en onderzwaveligzure natronGa naar voetnoot1) bij. Deze kleur overtreft in schoonheid verre de kleurstof bereid uit Pikrinzuur en Indigocarmin, maar is wegens hare hooge prijs alleen voor zijde te gebruiken. Anilingeel is een nevenproduct bij de bereiding van Anilinrood, dat weinig waarde heeft, in zooverre reeds voor de ontdekking | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
[pagina 428]
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
der Anilinkleuren het straks te vermelden pikrinzuur bekend was en volop gebruikt werd. Verhit men Girard's anilinviolet en zoutzuur anilin gezamenlijk tot 240o C., dan verkrijgt men Anilinbruin, hetwelk de modelkeur Havana oplevert. Het verwt wol zonder bijtmiddel. Ook komt een soort bruin in den handel voor, Naphta bruin genoemd, zijnde slecht gezuiverd anilinrood; men lost dit op in azijnzuur, de kleuren, die het geeft zijn echter niet echt. Het anilinzwart bestaat niet in den vrijen toestand, het wordt op den draad te voorschijn gebragt. Er zijn verscheidene recepten ter zijner bereiding. De ontdekker er van is John Lightfoot te Accrington, die er in 1868 patent op nam. Lauth bracht aan Lightfoot's methode eenige verbeteringen aan door te verbinderen, dat bij het drukken van anilinzwart de drukrollen aangetast worden en de draad in sterkte lijdt. Deze kleur is echter niet geschikt om wol te verven, maar laat zich uitmuntend bezigen tot het merken van goederen, die met chloorkalk gebleekt worden, daar het niet daardoor aangetast wordt noch door zuren. De methode van Lauth is weder overtroffen door die van een fransch werkman te Rouaan, Lucas genaamd, die zijn geheim aan de firma Petersen in St. Denis, Villeneuve la Garenne verkocht, zoodat nu deze een zwarte kleurstof in den handel brengt onder den naam van Noir d'Anilin Lucas. Het voordeel van deze boven de andere methoden is, dat zij een zwarte kleurstof als zoodanig levert, die weinig moeite in hare bewerking vordert. Eenige voor de industrie tot nog toe minder belangrijke anilinkleuren, die of uit het anilinrood of het anilinzwart bereid worden, ga ik stilzwijgend voorbij. Het gebruik der anilinkleuren in niet alleen beperkt gebleven tot het verven van weefsels, maar heeft zich uitgestrekt tot het kleuren van bontwerk, hoedveêren, kunstbloemen, speelgoed, leer, mandwerk, was- en paraffinkaarsen, enz. Dit gebruik bracht de vraag op het tapijt: zijn de anilinkleuren vergiftig? De ervaring leert, dat, minstens mechanisch, zij niet vergiftig werken, daar zij op de gezondheid der werkleiden in de fabrieken geen nadeeligen invloed uitoefenen. Maar het gebruik dat er nog verder van gemaakt wordt, waardoor zij in het spijsverteeringskanaal geraken, moet tot voorzigtigheid aansporen. In het dagelijksch gebruik komen tegenwoordig voor: likeuren met | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
[pagina 429]
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
anilinkleuren gekleurd, evenzoo confituren, vruchtensappen en vruchtenijs. Nu is volgens de onderzoekingen van Sonnenkalb anilin een heftig gif, kleine giften veroorzaken onpasselijkheid, grooten den dood. Zuivere anilinkleuren zijn niet vergiftig, maar in geval van onzuiverheid kan haar arsenik- of kwikgehalte giftig werken. Hoewel door het groote kleuringsvermogen dier lichamen het gevaar verkleind wordt, blijft voorzichtigheid aanbevolen. Voor het schilderen met olieverf zijn de anilinkleuren niet te gebruiken om hare geringe duurzaamheid. De zware steenkolenteer-olie - het destillaat dat tusschen 150o-200o C. van de steenkolenteer overgaat - bevat, zooals reeds gezegd is, hoofdzakelijk phenol en naphtalin. Het phenolGa naar voetnoot1), bekend onder den naam van steenkolenteerkreosoot, wordt gebezigd tot conservering van hout, maar voornamelijk ter bereiding der gele kleurstof, die pikrinzuurGa naar voetnoot2) heet. Deze werd reeds in de vorige eeuw ontdekt en verkreeg verschillende namen, de meest gebruikelijke is hier opgegeven. Het wordt bereid door phenol met salpeterzuur te behandelen, in het begin zonder hitte aan te brengen, daar de inwerking heftig is. Deze stof kleurt wol en zijde zonder bijtmiddel fraai geel. Linnen en katoen worden door haar niet gekleurd, het pikrinzuur kan dus als een herkenningsmiddel voor deze stoffen dienen en wordt ook als zoodanig gebruikt. Het andere hoofdbestanddeel der zware steenkolen teerolie, het naphtalin, was tot voor korten tijd bijna zonder waarde. Men bereidde wel uit zoutzuur naphtalamin - analoog aan hetzelfde anilinzout - door inwerking van salpeterigzure potasch roode en violette kleuren, maar zij moesten in deugdelijkheid wijken voor dezelfde Anilinkleuren. In Frankrijk leerde men vervolgens uit het naphtalin benzoëzuur bereiden en gebruikte daarvoor niet de stof, verkregen uit de zware steenkolenteer-olie, maar wat zich afzet in de buizen der gasfabriek. Dit laat zich n.l. gemakkelijk zuiveren door sublimatie. Het naphtalin zet zich dikwijls in groote massas in de wijde buizen af en verstopt deze wel eens. Het wordt toch bij 79o C. vast. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
[pagina 430]
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Uit het gezuiverde naphtalin wordt door omzettingen analoog aan die van het benzol tot anilin, naphtalamin - eene base verkregen. Door andere omzettingen - wier vermelding hier niet op hare plaats zoude zijn - wordt een prachtige geel tot oranje gekleurde stofGa naar voetnoot1) verkregen, die reeds in de ververij opgenomen is. Zij kleurt zijde en wol zonder bijtmiddel.
Ik eindig hier mijne beschouwing over de producten der drooge destillatie van steenkolen. Voorzeker is het een onderwerp, welks populaire voorstelling een der moeijelijkste is en zal daarom menige lezer van dit tijdschrift deze bladen oningezien laten. En kan men al niet beter verwachten, waar zoovele termen, onbekend in het dagelijksch leven, voorkomen in een opstel, dat voor een beschaafd, hoewel niet deskundig publiek gebracht wordt, hij, die niet geheel onkundig wil blijven van het drijven en werken op dit gebied, zal wel deze geringe moeijelijkheid te boven komen. Ik heb, zoo veel mogelijk, waar namen uit het gewone leven voorhanden waren, deze naast de scheikundige gezet. Voor vele was dit ondoenlijk; aldehijd heet toch niet anders dan aldehijd. Het verven is niet nader omschreven omdat, wie eene blauwververij ooit gezien heeft, - en wie het niet gedaan heeft doe het nog, - die op het oog eenvoudige maar in de praktijk ervaring vorderende bewerking heeft kunnen nagaan. Aanschouwen gaat bij deze zaken bovenal. Men moge in woorden nog zoo duidelijk de voorstelling eener zaak kunnen geven, praktijk laat zich niet in woorden zeggen. Nog dit eene: De afbeelding der trommel van den gasmeter is genomen naar eene oudere inrichting, maar met voordacht gekozen, omdat, naar mijn oordeel, zij de omwenteling der trommel duidelijker maakt, dan eene afbeelding der nieuwere constructie dit zou doen. Hoorn, April 1868. |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

