|
| |
| |
| |
V Witte cellen
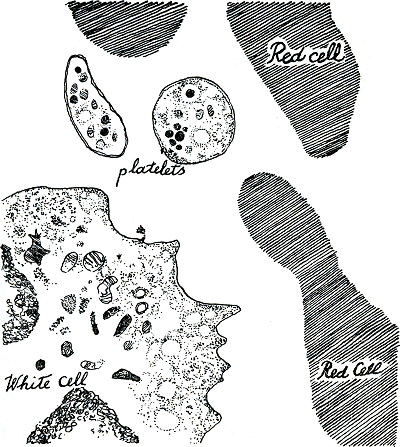
Als van een bonk kunstmatig hardgemaakt bloed een heel dun plakje wordt gesneden, dat dan alle beledigingen en vernietigende wreedheden ondergaat waarmee we zijn fijne structuur proberen te bewaren, dan zullen elektronenmicroscoop-foto's daarvan de rode cellen laten zien als donkere dorre eilanden verstijfd asfalt in een woestijn. Bloedplaatjes daartussendoor gezaaid zien er dan uit als bloemen vol verfijndheden. En zo om de vijfhonderd rode cellen vind je dan een
Figuur 48.
| |
| |
perk vol kralen en kant. Dat is een leukocyt, een witte cel. Daar zie je in figuur 48 een stukje van. Zelfs in een primitief uitstrijkpreparaat, gekleurd met Wright's kleurstof zoals in het vorige hoofdstuk, en door een doodgewone microscoop bekeken, springen de onaangesneden witte cellen van bontheid je oog in, zoals ze opbloeien in het saaie veld vol dofrode kleipannekoeken, de rode cellen.
Vijf soorten witte cellen kan je in zo'n eenvoudig preparaat makkelijk leren onderscheiden (figuur 49). Drie daarvan horen tot één gezin: de granulocyten, want hun protoplasma (alles van binnen behalve de kern dus) ziet er, onder een vergroting van duizend maal, zo korrelig uit als onvergroot griesmeel of rijst zelfs. Als dat griesmeel zich grijzig

Figuur 49.
paars heeft laten kleuren, een neutraal mengsel dus van het basisch blauw en het zure rood in de kleurstof, dan heet de cel een neutrofiel. Zijn de korrels groot en hebben ze zich met het eosine rood gekleurd, dan heet de cel een eosinofiel. En een cel vol grove, blauwzwartig gemaakte korrels heet een basofiel. Alle granylocyten hebben nogal gek gevormde, hier en daar ingesnoerde kernen, vooral de neutrofielen; ze worden daarom wel eens polymorfonucleaire granulocyten genoemd.
Je zult ook lymfocyten zien, cellen met nogal ronde donkere kernen, en een enkele monocyt, die meer lijkt alsof hij van platgedrukt, fijn doorzichtig schuim is gemaakt. Als het preparaat netjes ge-
| |
| |
maakt is zullen al die cellen, keurig van elkaar gescheiden, er zo rond en plat uitzien als beschilderde bierviltjes. Laat je niet belazeren. In een druppel vers bloed, met de fasemicroscoop bekeken, kan je bijvoorbeeld een gewone granulocyt eerst rond zien rollen als een glazen knikker, maar na een tijdje zal hij op het glas gaan zitten. Dan, alsof
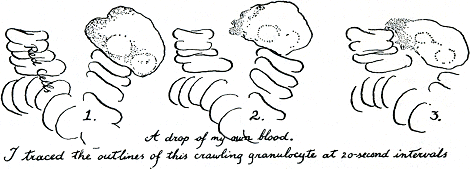
Figuur 50. Een druppel van mijn eigen bloed. Ik heb de omtrekken van deze kruipende granulocyt om de twintig seconden over getrokken.
hij eindelijk op zijn gemak is, zal hij beginnen rond te tasten: een heldere blaar zal ergens uit zijn flank komen, wat blijkbaar waterig geworden protoplasma zal die vullen met wild dansende spikkeltjes die dan weer trager worden wanneer de vloeistof rondom zich weer verdikt tot cellevlees. Weer een blaar, misschien een lange in dezelfde richting, en daar vult hij zich al weer op en wordt de cel een vaas, een weke knots die de vreemd toeschietelijke kern uitrekt tot een parelsnoer van drie parels. Dan, misschien door iets waaraan hij snuffelde geschrokken, krimpt hij zo plotseling als zijn stroperigheid dat toelaat ineen, een slordig spoor van uitgesmeerde protoplasmastaart achterlatend dat later als een balletje samentrekt en wegzeilt. Of, als een grazend konijn (figuur 50), kan hij zijn voorkant rondsnuffelend steeds verder van zijn achterwerk laten afdwalen dat dan tenslotte in een trage sprong moet meekomen. Net als kleine kinderen zitten dus deze witte cellen alleen maar zoet stil totdat ze aan een nieuwe omgeving zijn gewend; zodra ze zich thuisvoelen worden ze wild. Binnen jouzelf zou het gedrag zelfs van een zichtbaar gemaakte witte cel onmogelijk zijn te voorspellen. Meegesleurd in de bloedstroom maken de meeste zich zo klein mogelijk, dus bolvormig; maar zodra ze door iets worden aangetrokken gaan ze erbij zitten en beginnen ze te kruipen op een manier die typisch is voor elke soort cel. Er wordt hard in
| |
| |
laboratoria gewerkt om uit te vinden wat zo aantrekkelijk is voor welke cellen en waarom. Straks kan ik je iets vertellen over de geraffineerde smaak van de kleine ondiertjes.
Uit mijn eigen, heel geringe werk op dit gebied heb ik toch wel één ding geleerd: dat van het zichtbaar maken, een witte cel, net als een eiwitmolecuul, volledig verandert. Hij zal zich buiten ons lichaam gedragen volgens de wetten van de wereld die we hem voorzetten: in een lichtbundel gevangen tussen platen glas of plastic, of, slachtoffer van onze gemeenste fout, vermoord en geverfd en gebalsemd. Het is geen wonder dat zelfs dan de cel nog mooi is om te zien. Hij was door de natuur gemaakt, en ook dood gehoorzaamt hij nog aan onzichtbare wetten van de natuur, zoals alle schoonheid. Zoals in elk goed kunstprodukt, is er zoveel werkelijkheid uit hem weggelaten dat het overschietend skelet mager genoeg is om te kunnen worden bewonderd en eenvoudig genoeg om ons wijs te maken dat we het kunnen begrijpen. De zotste vooroordelen kunnen door die versimpelde geverfde cellen worden verwekt. Ik kan nooit laten de hoekige korrels in de basofielen, zo erg donker gekleurd, keihard als gebroken kiezels te zien; en de gladde korrels in de eosinofielen, zo oranje, zo zuigjesachtig kan ik me niet anders dan zuur voorstellen in plaats van basisch. Als we maar eens dichter en dichter bij een druppel bloed konden komen, en desnoods daar kleiner en kleiner bij worden, hoeveel zou er dan overblijven van zijn eens zo kennelijk bloederige eigenschappen? De uitwendige druppelvorm verdwijnt zodra we binnenkomen, zijn kleur wordt eerst bleek geel en dan, dieper binnen, wordt het door alle rode cellen gefilterde licht weer roder. Maar dan, nog kleiner geworden, voelen we de natheid rondom ons verdwijnen en glippen we tussen de watermoleculen door. En dan verliezen zelfs de wanden van rode en witte cellen hun vastheid en gaan voor ons open als kraalgordijnen, om ons te tonen dat die oude werkelijkheid der dingen, eens zo standvastig van elkaar gescheiden, niets anders was dan een onhandige en onscherpe tijdopname van een wilde en onbegrijpelijk ingewikkelde dans. Het is al
erg genoeg dat we niet kunnen zien hoe klein de belangrijke dingen zijn; maar het is nog erger dat we ze helemaal niet kunnen zien omdat ze daarvoor te kort duren. Konden we een miljoen maal een miljoen maal sneller kijken, dan zagen we het water als een wereld van doorzichtige groeiende en brekende dingen rondom dingen. Maar nee, we zien niets dan een
| |
| |
veeg, een film waarvan alle foto's tegelijk in onze trage ogen terecht lijken te komen; een langzaam dood gemiddelde voor onze langzame, lang levende hersens. Zelfs voor een klein, kort levend virusdeeltje is een mist van een minuut een leven lang vol droge en kletsnatte seizoenen.
Ik hoop dat ik je met deze lange alinea heb voorbereid voor een toch wel allerduidelijkst mysterie waar ik in het vorige hoofdstuk omheen heb gepraat: hoe komen de nieuw gevormde cellen, buiten het bloed geboren, ooit in dat overal afgesloten systeem van bloedvaten terecht? Eenmaal daarin gevangen, zullen de meeste rode cellen niet ontsnappen tot ze zich kapotgestorven hebben. Zelfs de meeste eiwitmoleculen kunnen of willen niet door de bloedvatwanden heen. Maar het geweldige lijf van een neutrofiel glipt erdoor zonder maar een spoor van lekkage achter te laten. Het kost mij de minste moeite om in zo'n voldongen feit te geloven als ik mij verbeeld er zo dicht bij te zijn dat ik moleculen aan het werk kan zien. Dan kan ik mij bijvoorbeeld indenken dat speciale eiwitmoleculen samen met de gerangschikte membraan-fosfolipiden van zowel de neutrofiel als van een paar endotheelcellen in de bloedvatwand zich werkelijk als kraalgordijnen gedragen. Dat van de een zou zich kunnen uitspreiden over, of zelfs eventjes vermengen met dat van de ander. Zolang de lichaamsmoleculen of moleculaire complexen van ieder zijn eigen gordijnpatroon maar blijft herkennen, kunnen twee cellen zonder hun identiteit uit het oog te verliezen behoorlijk intiem zijn. Het membraan van de ene cel zou zelfs wel om dat van de andere heen kunnen kruipen, en tussen twee endotheelcellen zouden de membranen een soort van ritssluitingachtig oppervlak kunnen maken, waarin tijdelijke gapingen door wriemelende leukocyten zouden kunnen worden gemaakt en verplaatst, zodat de vaatwand zich achter ze sluit als een oerwoud waarin zelfs een olifant spoorloos wegtrekt.
Eigenlijk is van het witte-celmembraan weinig bekend. Het protoplasma is zoveel dikker en zo vol mooie delicate voorwerpjes dat het veel meer onderzocht is. Daarin zijn dan ook stoffen, enzymen vooral, gevonden die typisch genoeg zijn om hun gastheercel te onderscheiden. Maar zolang we niet goed weten waar en wanneer zo'n enzym in zo'n cel actief is-en dat soort onderzoek is nog erg jong-is het catalogiseren ervan zoiets als alle werkwoorden uit een boek halen en op een rijtje zetten. Actie zonder betekenis.
| |
| |
Maar ik mag je ook niet de indruk geven dat alleen het onzichtbaar kleine detail iets van de celfuncties kan vertellen. Zelfs doodgewoon tellen, om te zien wat voor soort cellen waar en wanneer verschijnen, moet ons iets vertellen. Hier dus in het kort een beschrijving van dat soort primitieve techniek.
| |
Witte cellen tellen
Het moeilijke van witte cellen tellen is dar er vijfhonderd tot duizend maal meer rode cellen zijn. Gelukkig hemolyseren die (figuur 41, weetje nog wel) onder de juiste omstandigheden veel gemakkelijker dan de witte cellen, dus als je nog eens naar de beschrijving van rodecellentellingen kijkt kan je zelf wel een paar kunstjes bedenken om de witte mee aan te vallen.
Zoals je misschien geraden hebt, kan je een druppel vers bloed in een speciale witte-celpipet opzuigen tot een streepje, en de rest opvullen met een erytrocyten-vernietigende oplossing. Vaak wordt daar azijnzuur voor gebruikt, vandaar de slalucht in zo'n lab soms. De pipet verdunt je bloed maar twintig keer (in plaats van tweehonderd zoals in de ‘rode pipet’). Je weet al hoe de telkamer gevuld wordt; alleen moet ditmaal een groter oppervlak worden geteld, en dan nog is een fout van 20% te hoog of te laag, redelijk. Ik hoop dan ook dat deze methode binnenkort nog alleen maar door opgezette poppen in een museum zal worden vertoond. De machine die rode cellen telt, kan ook witte tellen en in een groot volume, dus nauwkeuriger; zoals hij nu is moet hij alleen nog wat beter leren zich op zijn eigen vergissingen te betrappen, en niet zo vervelend alle stofdeeltjes mee te rekenen. Hoe dan ook behoor je normaal vijfduizend tot tienduizend witte cellen per kubieke millimeter te vinden.
Voor de zogenaamde complete bloedtelling waar doktoren soms om vragen heb je meer nodig dan hematocriet, hemoglobine en totale celtellingen; er moet ook tussen de verschillende soorten witte cel gedifferentieerd worden, en daarvoor moeten uitstrijkjes worden gemaakt en gekleurd. Die moeten dan ‘gelezen’ worden door ze langzaam zig-zag op en neer en heen en weer te schuiven in de microscoop en elke cel te noteren die je langs ziet komen, bijvoorbeeld door op een rij knoppen te drukken die elk een telapparaatje voor de overeenkomstige soort witte cel bedienen. Meestal belt zo'n rijtje als het to-
| |
| |
taal honderd is, want dan geeft elk raampje erin het percentage van elke soort getelde cel aan. In bloed van een normale westerse volwassene die zich de laatste tijd niet teveel heeft opgewonden en geen wormen heeft, zal je dan wel ongeveer 55 tot 60 percent volwassen neutrofiele, 2 percent eosinofiele en minder dan 1 percent basofiele granulocyten, 25 tot 35 percent lymfocyten van allerlei formaat, en 5 percent monocyten vinden. Natuurlijk moet je, om die getallen zoals twee of bijvoorbeeld een half percent van iets betekenis te geven, meer dan honderd en misschien zelfs meer dan duizend witte cellen geteld hebben, dus voor de zeldzame vormen zijn methoden bedacht om ze rechtstreeks te tellen, in een telkamer, door ze te kleuren en alle andere cellen te vernietigen.
Doordat meestal het percentage neutrofiele granulocyten en lymfocyten dat je in een uitstrijkje tegenkomt zo groot is, kan de telling daarvan nog meer worden gedifferentieerd: in percentages jongere en oudere cellen. Elke soort vormt zich meestal in zijn eigen wereld: de granulocyt in het beenmerg, de lymfocyt in de lymfklieren, de monocyt in een soort weefsel dat het reticulo-endotheliaal systeem genoemd wordt en waarvan veldjes leven in de milt, de lever, en andere moerasachtige streken. Waar ze ook worden geboren, de witte cellen moeten afstammen van ‘primitieve’ stamcellen, grote cellen meestal, met grote ronde kernen. Die cellen moeten op een of andere manier jong blijven terwijl toch de cellen die ze door deling vormen, nog verder door moeten gaan met zich te delen om steeds meer op de bedoelde volwassen vorm te lijken en dan het bloed in te gaan. Maar de stamcel blijft thuis. In 1904 publiceerde Arneth een schema waarin de jongste granulocyten links en de oudere rechts stonden. Natuurlijk, want we lezen toch ook in die richting (figuur 51); maar sindsdien noemen we een telling die abnormaal veel jonge cellen vertoont, een bewijs van een ‘verschuiving naar links’. Die geeft aan dat de cellen met abnormale haast gevormd en het bloed in geduwd zijn, en geeft de indruk dat ze speciaal nodig waren voor wat er aan de patiënt
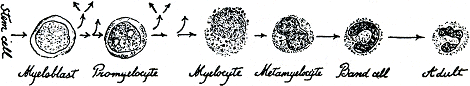
Figuur 51.
| |
| |
mankeert, of dat er iets gemaakt wordt door zijn zieke lichaam dat speciaal dit soort cellen slacht of dat soort stamcellen prikkelt, of wat dan ook.
Gelukkig heeft het vinden van sommige specifieke cellen geleid tot sommige meer specifieke ideeën dan deze.
| |
Granulocyten: neutrofiel, eosinofiel en basofiel
De stappen van stamcel tot volwassen neutrofiel hebben zich laten tellen. De stamcel deelt zich een keer om een myeloblast te vormen. Die deelt zich, en elk van de twee deelt zich weer om in totaal vier promyelocyten te maken; elke promyelocyt deelt zich twee maal om een groepje van vier myelocyten te produceren; drie uur later is elke myelocyt een metamyelocyt geworden; negen uur later heeft elke metamyelocyt zijn kern tot een band vervormd en wordt dus bandcel genoemd; en een dag later is de band dat gekke knobbelige ding geworden waaraan we de volwassen neutrofiel herkennen; nu mag hij op weg zijn naar het bloed, maar doet daar meestal nog drie dagen over. De tijden van dit programma zijn gevonden door jonge cellen radioactieve isotopen te laten drinken, en dan te kijken waar en wanneer de activiteit later te vinden is, naarmate de cellen ouder worden.
De granulocyten van verschillende soorten zoogdieren zien er verschillend uit. De neutrofielen van ratten hebben vaak een slangerige en bijna ringvormige kern, en die van konijnen en Guinese biggetjes hebben korrels die zich met eosine nogal oranje kleuren en daarom ‘pseudo-eosinofielen’ genoemd worden. Ik heb eens een tijdje naar bloed van chinchilla's gekeken, dat had ook beslist iets onmenselijks; ze beten trouwens nogal graag.
Die laatste drie dagen voordat de al volwassen neutrofiel het beenmerg uit springt en het bloed in, zou in Amerikaanse ruimtetaal een ‘final hold before switching to automatic count-down, with all systems go’ genoemd kunnen worden. Alles is klaar en wacht op het laatste commando, en dat wacht op het juiste moment: wanneer de buitenwereld erom vraagt. Van een hond met A circulerende witte cellen kan men zeven keer A witte cellen wegnemen in een enkele operatie, zodat het beenmerg en zo, zes maal zoveel leukocyten in voorraad gehad moet hebben dan op dat ogenblik rondstroomden in het bloed. Maar dat ‘rondstromen’ kan langs ingewikkelde paden ge-
| |
| |
beuren. Terwijl je dit rustig zit te lezen, zitten misschien ongeveer de helft van je granulocyten tegen je bloedvatwanden geplakt te wachten. Als er iets gebeurt zwermen die los en laten zich weer meevoeren. Trouwens, meestal bezoeken ze je bloed maar ongeveer tien uur, en lopen dan door de wanden heen weg. Dat betekent dus eigenlijk dat je, statistisch gesproken, meer dan twee maal per dag een nieuw stel granulocyten krijgt-maar dat gebeurt natuurlijk niet echt in dag- en nachtploegen. Ik vind het eigenlijk zo lief, zo'n cel die eerst drie dagen zit te wachten op zo'n reisje en dat is dan zo kort.
Waar gaan ze heen na dat korte bezoek? Hun lijken worden gevonden in de longen, en stukken belanden in de lever en de milt zonder een helder spoor na te laten van hun zo korte avonturen. Ze zullen meestal wel zijn weggezworven, achter een verre roep aan, misschien de schreeuw van een stof die door een geïnfecteerde wond was uitgezonden. Had die stof lang genoeg geroepen, dan hadden zij de richting kunnen vinden naar zijn toenemende sterkte, en het slagveld kunnen bereiken, waar ze de oorzaak van de ramp, de bacteriën, levend zouden hebben opgevreten, met nog hele stukken rottend weefsel erbij, want die zijn dan bedekt met een speciaal voor witte cellen heerlijk soort eiwit, zoals je later zult zien. Onder de maaltijd en daarna moet zo'n cel heel wat enzymen gebruikt hebben: lipase voor vet en proteasen voor eiwitvertering, maar ook een ander soort enzymen, om de brandstof mee aan te steken waarvan zijn fysische systemen blijven leven, zijn pseudopodiën blijven vingeren en omhelzen. En er is werk nodig om zijn eigen membraan mee te repareren, want zijn vellerige vingers zullen elkaar wel eens grijpen en met het voedsel naar binnen proppen waat hij zijn eigen afgesnoerde huidplooien zal moeten verteren. Als de neutrofiel zich ondraaglijk vol heeft gegeten wordt hij ziek en begint kleine hompjes korrelig protoplasma los te laten voor hij sterft. De hompjes zullen nog een tijdje rond blijven zweven, en worden dan op hun beurt verslonden door de later gearriveerde lymfocyten. Hier, waar de ontsteking is, maar ook in de milt en op andere plaatsen waar stukjes granulocyt hun einde vinden na een lange tocht, komt een grote verandering over de lymfocyten en plasmacellen die deze resten van het vreemde voedsel in de dode granulocyten herkauwen... maar daarover meer onder het stukje over lymfocyten. Als je wilt kan je misschien net zo makkelijk daarop overspringen, terwijl ik hier intussen doorga met
| |
| |
de andere soorten granulocyt, alleen maar om hun gezin bij elkaar te houden.
Als ik zeg dat maar twee percent van je witte cellen eosinofielen zijn, moet je ze dan zeldzaam noemen? Ik vind het altijd nogal typisch en kinderachtig van populair-wetenschappelijke schrijvers als ze proberen je te vertellen dat getallen heus leuk zijn. Want meteen beginnen ze dan zelf alles voor je uit te rekenen en dan is de verrassing of grap er al af. Probeer dus zelf eens, met de cijfers die je al hebt: zoveel witte cellen, daarvan zoveel percent, enzovoort; vraag bijvoorbeeld hoeveel afstand er ligt tussen twee eosinofielen gemiddeld, of hoeveel je er alles bij elkaar hebt.
Om eosinofielen te tellen in een telkamer, moet je ze meer dan alle. andere cellen zichtbaar maken. Dat wordt gedaan met een verdunningsvloeistof waarin een kleurstof is om ze te kleuren, alkali om alle andere witte cellen stuk te maken, en een stof met hoge brekingsindex om de rode cellen zo onzichtbaar te maken als glazen kralen in water. Ditmaal verdun je het bloed maar tienvoudig en tel je een extra groot oppervlak. Deze methode bleek goed genoeg om bijvoorbeeld te ontdekken dat tegen de tijd dat je 's ochtends opstaat, het aantal eosinofielen in je bloed op zijn laagst is. Sommigen, in tegenstelling tot anderen, denken gevonden te hebben dat die daling niet voorkomt in blinden en veroorzaakt wordt door licht op een bepaald gebied van je netvlies. Er is wel een belangrijke gebeurtenis onder in je hersenen die beslist van belang is: daar zit je hypofyse en maakt, onder andere, Adreno Cortico Troop Hormoon (acth). Dat dwingt de buitenlagen van je bijnieren (klieren die op je nieren zitten) om cortisonachtige hormonen te maken, en op een of andere manier maken die dat je circulerende eosinofielen zoek raken. Dat is erg handig voor doktoren die willen weten hoe goed je bijnieren reageren: ze laten een ‘eo's’-telling op je doen voor en nadat ze wat acth in je hebben gespoten; dan moet er een daling gevonden worden.
Er zijn een hoop soorten van spanning: schik, schrik, schaamte, schoppen en schateren, allemaal gaan ze samen met een toename van je acth, maar ik weet helemaal niet of het misschien wel stukspatten van je eosinofielen je pret moet verhogen of alleen maar verdraagbaar maken. Dit alles zegt je trouwens niets over de functie van die cellen. Ik kan je nog wel meer inlichtingen geven waar je bijna evenveel aan hebt: het aantal circulerende eosinofielen neemt geweldig
| |
| |
toe bij allergische reacties zoals astma, en na inspuiten van heparine, of histamine, of een uittreksel van de ‘gewone spoelworm’ (Ascaris) (een parasitische engerd), of asbest. Bij allergische reacties wandelen de eosinofielen blijkbaar naar gebieden waar antigeen het meest met antilichamen reageert. Tussen al die ontdekkingen zal wel een logisch verband bestaan. Bijvoorbeeld: bijnierschorshormonen onderdrukken allergische reacties zowel als het aantal circulerende eosinofielen. En wat asbest betreft: vaak moeten in een lab oplossingen steriel gemaakt worden (om voor inspuiten te gebruiken) door ze te filtreren door dikke schijven asbest, en de vezeltjes die daaruit losraken en de oplossing beviezerikken veroorzaken dan een bloeitijd van eosinofielen in de ontvanger, waarvoor natuurlijk de oplossingen vroeger per ongeluk de schuld kregen. Wat ik hiervan vooral leuk vind is dat het om vezels gaat die iets voor deze cellen betekenen, want er is een meer natuurlijke vezel waar eosinofielen dol op schijnen te zijn: fibrine. En tenslotte is het effect van heparine en van histamine ook interessant: allebei komen in basofiele cellen voor, en er is ontdekt dat overal waar basofielen kapotgaan, eosinofielen verschijnen.
Basofielen zijn wel het meest opvallend, vooral als ze hun korrels laten kleuren en zo donker worden als een hagelwolk, maar een goede manier om ze rechtstreeks, nat, te tellen is nog maar pas uitgevonden. Nog moeilijker is het, natuurlijk, ze te verzamelen voor chemische analyse. Nu wil het geluk of ongeluk dat er een soort cel in je weefsels bestaat die mestcel wordt genoemd, en mestcellen, vooral als woekeringen, kunnen lekker worden verzameld en bestudeerd, maar niemand weet of ze identiek of zelfs nauw verwant zijn met basofielen in het bloed. Allebei, net als de eo's, nemen af in spanning, in de morgen, en na gebruik van corticosteroïden; tenminste, het lijkt alsof hun aantal afneemt, maar eigenlijk verliezen hun korrels misschien alleen maar hun kleurbaarheid. En als je rekent dat daaruit, zoals ik zei, waarschijnlijk heparine en histamine komen en dat die eosinofielen aantrekken, nou dan. Tot overmaat van samenhang schijnen de korrels van eosinofielen ook nog invloed op basofielen te hebben.
Het hinderlijke van basofielen is dat ze zulke beroemde stoffen produceren zonder te zeggen waarom. Histamine doet iets met je capillairen en je darmen, en kan je hoofdpijn bezorgen zelfs zonder dat je het bestudeert. Heparine remt de bloedstolling op enige manieren, maar maakt ook lipase (dat vetsplitsend enzym) uit een onactief
| |
| |
plasma-eiwit. Het lipase splitst vet zodat er vetzuren uit vrijkomen, en die kunnen hemolyse van de rode cellen veroorzaken maar worden gelukkig meteen door albumine opgepikt.
Ik heb gelezen dat er nog steeds vijfentwintig theorieën over de functie van basofielen bestaan. Nu kan je zelf misschien wel een zesentwintigste maken.
| |
Lymfocyten, plasmacellen en immuniteit
Uit de literatuur krijg ik op het ogenblik de indruk dat de voorouder van een lymfocyt zich een keer deelt om een lymfoblast te maken, en dat die zich drie maal deelt om een troepje grote lymfocyten te maken; elke grote lymfocyt maakt dan door twee delingen vier middelmatig grote lymfocyten die elk weer een groepje kleine lymfocyten maken (zoals in figuur 52). Dat gebeurt allemaal in lymfklieren, milt,
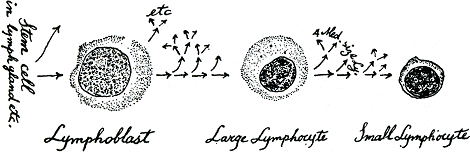
Figuur 52.
en andere plaatsen, beenmerg inbegrepen. Al die cellen worden door de lymfvaten het bloed in gegoten met een snelheid die groot genoeg zou zijn om al je lymfocyten enige malen per dag te vervangen, en je zou dus denken dat je bloed ze ongelooflijk snel opeet-maar nu is gebleken dat ze stiekem het bloed uitkruipen en terug de lymf in, en van daar weer het bloed in worden gesleurd. Zo'n 8-vormige verkeersbaan verklaart waardoor geleerden, maar naar een klein stukje verkeer kijkend, niet merkten dat dezelfde kereltjes enige malen langskwamen, en de levensduur van een gemiddelde lymfocyt is daardoor geschat op een paar uur door sommigen en een paar maanden door anderen. Maar waar gaan ze eventueel naar toe? En wat doen ze?
Het is eigenlijk wel zeker dat lymfocyten antilichamen maken,
| |
| |
maar daarin gaan ze waarschijnlijk niet tot zulke uitersten als de plasmacellen. De plasmacellen (figuur 53) groeien op in het beenmerg en komen op den duur terecht in plekken die geïnfecteerd zijn, maar worden haast nooit in het bloed zelf gevonden. Ze hebben veel protoplasma, dat door Wright's kleurstof onvergetelijk blauw wordt gekleurd.

Figuur 53.
Blauw is basofiel, basofiel is zuur, en het zuur is ribonucleïnezuur, en dat betekent: eiwitfabriek. In de elektronenmicroscoop ziet een dun plakje van de plasmacel er zo uit (figuur 54):
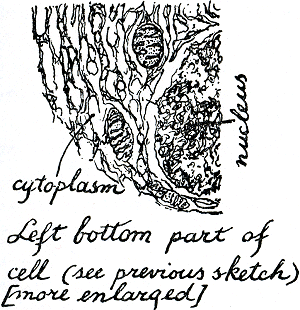
Figuur 54.
Dat is maar een stukje doorsnede van wat oorspronkelijk een heel nest van laag op laag vol keukenplankjes vol korreltjes moet zijn, elk korreltje enzymen dragend en allemaal op rijen als flessen in de kast van een chemielaboratorium; alleen, hier in de cel zitten de chemicaliën misschien meestal buitenop de flessen. Nou, daar zitten ze dan.
| |
| |
Als de fabriek werkelijk antistoffen moet maken, hoe krijg je hem dan aan het werk? De eerste stap moet de cel waarschijnlijk al zelf doen: van de vreemde, te bevechten stof moet eerst een flinke hap genomen worden, zodat de plasmacel er eens goed met zijn protoplasma naar kan kijken. De hap die hij neemt is misschien wel een propje gebroken granulocyt, als een pil met een beetje van de vreemde stof, destijds door de levende granulocyt gegeten, er nog in. Die stof wordt nu een oplossend antigeen, en heeft diepe invloed op de plasmacel of lymfocyt die hem opat. Lymfocyten worden helemaal groot en weer jong van de ervaring.
De stof moet voor de etende cel een of ander kennelijk vreemd trekje hebben. Dat trekje moet nogal standvastig zijn, want de antistof die ertegen moet worden gemaakt behoort er sprekend op te lijken, en vage foto's lijken op te veel mensen tegelijk. Moleculen met stijve ringen van zes koolstofatomen kunnen erg goed poseren, maar lange aldoor maar heupwiegende ketens, zoals verzadigde vetzuren, kunnen dat niet en geen goede antistoffen kunnen tegen ze worden gemaakt. Moleculen die te klein zijn moeten zich op een groter molecuul, een eiwit, vasthechten om dan als een typisch gelaatstrekje van dat grotere molecuul herkend te worden als ‘vreemd’. Een geheel eiwitmolecuul kan natuurlijk ook als vreemd worden erkend.
Prachtig, maar hoe herkent zo'n plasmacel of lymfocyt dan een nooit-geziene stof als vreemd, of, nog nauwkeuriger en verbazingwekkender uitgedrukt: hoe herkent hij al die duizenden soorten eiwit van jouw eigen lijf als niet-vreemd? Misschien heeft de thymusklier daar iets mee te maken. Dat is een bleek slap ding dat in je borstkas kleiner begon te worden sinds je tien jaar oud was. Zelfs nu nog prikkelt het waarschijnlijk het maken van antistoffen. In piepjonge zoogdieren kan van alles worden ingespoten zonder dat antistoffen worden gevormd, en de thymus is dan nog erg klein, misschien te klein om iets aan de gang te krijgen. Alles wat dat kleine diertje dan, voordat zijn thymus begint te groeien, krijgt ingespoten en al zelf had noemt het daardoor ‘ikke’ en zal het altijd ‘ikke’ blijven noemen. Zelfs later, als de thymus al ontwaakt is en daarmee de antistoffenfabricage, en nog later als de thymus alweer inkrimpt, kan zo'n toch eigenlijk vreemde stof, eens als baby in het lijf gekregen, nog steeds worden herinnerd. Na jaren van afwezigheid weer ingespoten, wordt het goedje door de nu volwassene met een juichkreet: ‘Ikke!’ begroet
| |
| |
en hoeft niet bang te zijn ooit door antistoffen te zullen worden aangevallen. Niet dat hiermee alles ineens duidelijk wordt; maar het mysterie hangt nu tenminste nogal redelijk aan elkaar, en het lijkt niet zo gek dat ons lichaam een zekere leeftijd en wijsheid moet hebben bereikt voordat het zelf mag bepalen wat het zelf is en wat niet. Nadien wordt niets nieuws meer als vriendelijk beschouwd, en zoals hooikoortslijders je kunnen vertellen, worden zelfs de meest onschuldige moleculen soms aangevallen met belachelijke woede. Zelfs het eiwit van je eigen ooglens-want dat is in eenzaamheid ontstaan, zonder ooit door bloed te zijn gezien-wordt een antigeen als het ooit per ongeluk zijn afgesloten wereld verlaat en door lymfocyten of plasmacellen wordt opgemerkt. En dan heb je kans dat je eigen lichaam antistoffen daartegen maakt en daarmee je andere lens aanvalt.
Op het ogenblik worden veelziekten beschouwd als ‘auto-immuun’. De patiënt die aan zo'n ziekte lijdt moet op een of andere manier plotseling het gezicht van een van zijn eigen eiwitten zijn vergeten, en in de poging van zijn lichaam om dat eiwit dood te slaan vermoordt het zichzelf. Misschien is dat de schuld van het eiwit, is het ergens gekneusd tot een onherkenbaar iets of uit zijn normale isolatie losgebroken, maar het kan evengoed een geheugenverlies van de lymfocyten en plasmacellenfabriek zijn.
Er is meer reden voor het gebruik van dat woord ‘geheugen’ dan je misschien denkt. Het is namelijk best mogelijk dat er niet zo erg veel verschil is tussen het geheugen van je plasmacellen, dat van je hersenen en dat van je hele lichaam dat zichzelf van de ene dag op de andere herkent. Het schijnt ongeveer een half uur te kosten om de bron van een nieuw eiwit te bouwen-nodig voor het maken van een nieuwe antistof. Ook zal na een voldoend flinke elektrische schok een zoogdier alles vergeten wat minder dan een half uur voor die schok gebeurde. Met andere woorden: in beide gevallen wordt iets herinnerbaars gebouwd in een half uur.
Nu denk je misschien dat die geweldige lijst van antigenen waartegen je hebt leren vechten, een precies even lange lijst van even verschillend gekronkelde antistoffen in je moet hebben verwekt. Niks hoor: al je antistoffen horen tot de klasse van gammaglobulinen, en die bestaan allemaal uit twee lange ketens die A, en twee korte die B genoemd worden, alle vier samengehouden door S-S-banden, zo:
| |
| |
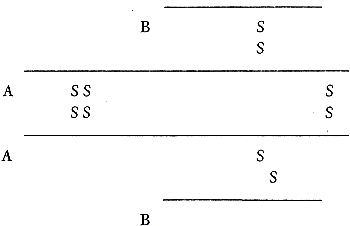
Zonder zijn B-keten is een A-keten niet actief.
Toch bestaan er twee, heel ongelijke, groepen antilichamen: de eerste moleculen die je maakt, na je eerste contact met een nieuw antigeen, zullen een moleculair gewicht hebben van meer dan een miljoen; later, als je hetzelfde antigeen weer binnenkrijgt en herkent, maak je veel kleinere moleculen antistof, maar veel meer ook. Precies dat feit-dat je tweede reactie zo heel anders is dan je eerste, hoe lang geleden je die ook had-bewijst hoe goed en hoe onaanvechtbaar dat geheugen van je lymfocyten en plasmacellen is. Wat voor vorm het heeft: een beetje van het echte oude antigeen zelf, ergens ingekapseld? een stukje nucleïnezuurmachine dat een oude code vasthoudt en alleen maar persklaar om eenvoudig antistofmoleculen te drukken als daarnaar gevraagd wordt? Dat weet nog niemand.
In het vierarmige ding, hierboven afgedrukt, komt niet veel helix voor. Een bundel grillige ketens dus, waarvan de vorm bepaald moet worden door twee heel verschillende dingen: hij moet precies op dat persoonlijke profiel van het antigeen passen, maar hij moet ook bepaald worden, zoals in elk eiwit, door de nauwkeurige volgorde en aard van zijn aminozuurgroepen. Hoe kan dat gedaan worden?
Plasmacellen, buiten het lichaam gekweekt, geven de indruk dat het antigeenmolecuul, de plasmacel binnenkomend, inderdaad de stofwisseling daar zo verstoort dat de cel voortaan niets anders meer kan doen dan met zijn verbochelde codesysteem de ene antistof te maken tegen dat ene antigeen; alsof de sleutel tot een slot een kast heeft geopend vol met dezelfde sloten. Maar niet in alle proeven gedragen de cellen zich zo eenkennig: sommige maken wel degelijk verschillen-
| |
| |
de antistoffen tegelijkertijd. In een gesensitiseerd (gevoelig gemaakt, al antistof vormend) beest gaat het drukken, stempelen of wat je het dan ook noemen wilt, van antistof verbazend vlug: geef het eerst radioactieve aminozuren, en dan wat van het antigeen, en dertig minuten later heeft het al radioactieve antistof in zijn plasmacellen, en weer dertig minuten later heeft het al vrijgekomen radioactieve antistof in zijn bloed. En in wat voor hoeveelheden! Na een injectie van antigeen worden ongeveer honderdduizend moleculen antistof per seconde gevormd. Maar zodra daardoor al het omringende antigeen gebonden is, houdt de produktie van antilichamen op. Tenminste, in zo'n kweeksel van cellen buiten het lichaam. Binnen je lichaam gaan de twee waarschijnlijk niet zo netjes gelijk op, en leeft je overgeschoten antistof even lang als andere globulinen, met een halveringstijd van zowat vijftien dagen, of langer als je groter, korter als je kleiner bent dan een mens.
Nu denk je van dit alles misschien: in ieder geval, hoe ingewikkeld de reacties ook zijn die leiden tot de gebeurtenis, de reactie zelf tussen antigeen en antilichaam is zo eenvoudig als a+b=c. Hm. Soms misschien wel, en ik kan me best voorstellen hoe een bacil eenvoudig stikt door al het b op zijn a, maar met zo'n eenvoudige complexvorming kan weer een heel andere serie gebeurtenissen beginnen. Bijvoorbeeld, als zich maar acht moleculen antilichaam aan antigene plekken van de bacil vasthechten, wordt het beestje al meteen aantrekkelijk voor eosinofielen en neutrofielen, en zal het worden verslonden. Die lekkere sterke smaak komt waarschijnlijk niet van de antistof zelf (anders zouden de witte cellen zo al gek worden van eetlust), maar door het staartje van een optocht van een andere groep eiwicten, die allemaal ‘complement’ heten. Het volgende is dan gebeurd: toen de antistof zich verenigde met het antigeen, werd door die gebeurtenis een van de complementen, C'i geheten, aangetrokken; eenmaal geadsorbeerd veranderde dat in een enzym en adsorbeerde en veranderde het andere complementmoleculen; het laatste daarvan was voor de witte cellen het lekkerst.
| |
Meten van en met antigeen-antilichaamreacties
Zelfs als een antigeenmolecuul gewoon rondzweeft in het plasma zonder deel van bijvoorbeeld een bacilmembraan te zijn, kan het door
| |
| |
zich te combineren met een antilichaam-molecuul, complement vastgrijpen, of zoals dat officieel heet, complement fixeren. Maar complement dat kan meedoen aan zo'n reactie als die welke aan het oppervlak van een rode cel gebeurt, dus bijvoorbeeld tussen een bloedgroepstof en zijn antistof, heeft een dramatische kracht: daar veroorzaakt complement hemolyse van de hele cel. Dat is natuurlijk heerlijk zichtbaar voor mensen die daarmee willen werken. Je kan bijvoorbeeld een onbekende hoeveelheid antigeen laten reageren in oplossing, met een bekende hoeveelheid antilichaam in de aanwezigheid van een bekende hoeveelheid complement. Wat er na de complexreacties aan complement overblijft, hangt af van de hoeveelheid die gefixeerd werd (en die hangt weer af van de gezochte hoeveelheid antigeen), en kan op zijn beurt weer gemeten worden naar de hoeveelheid rode cellen (uitgedrukt in vrijkomend hemoglobine) die het nu nog kan laten hemolyseren als je er meer antistof en antigeen, en nu ook rode cellen, bij doet. Dat klinkt nogal ingewikkeld, maar je zult zelf nog wel ingewikkelder proeven kunnen bedenken. Het zijn allemaal complement-fixatieproeven.
Er zijn ook nog heel wat eenvoudiger immunologische proeven om niet-immunologische vragen mee op te lossen. Hier is er een die dr. Ratnoff gebruikt om factor xii (zie hoofdstuk i) te meten. Gezuiverd mensen-xii wordt in een konijn gespoten. Dat maakt er antistoffen tegen. Maak nu een suspensie van gewassen en chemisch behandelde rode cellen van een of ander zoogdier, of gebruik een suspensie van plastic poeder (‘latex’). Doe daar wat anti-xii van dat konijn bij; er zal wat van op het oppervlak van de gesuspendeerde deeltjes gaan zitten. Was die een paar maal in isotonisch zout water, en doe dan bijvoorbeeld wat normaal mensenplasma erbij. Het daarin voorkomende factor xii zal zich dan vasthechten op het al geadsorbeerde anti-xii en de deeltjes zullen samenklonteren. Het geklonter zal afhangen van de hoeveelheid xii in het mensenplasma, en kan dus als meting gebruikt worden. Je kan ook kunstmatig factor-xii-arm mensenplasma maken door er doodleuk konijne-anti-mensen-xii in te gooien; dat bindt dan de xii en maakt hem onwerkzaam. Maar al die proeven zijn niet beter dan het antiserum of-plasma dat je gemaakt hebt; en dat is nooit beter dan de zuiverheid van het antigeen dat je bij het beest hebt ingespoten; en helemaal zuiver is dat nooit. Bovendien zijn niet alle antistoffen even kieskeurig; sommige reage-
| |
| |
ren ook wel met iets verkeerds.
Een ander, nu heel bekend soort proef: maak een laag agar-gel, en daarin een krans van kleine gaatjes, ongeveer zes, rondom een centraal gaatje. Doe, bijvoorbeeld, druppels van allerlei jou bekende antisera in de krans van gaatjes (elk één serum natuurlijk), en een oplossing van onbekende eiwitten in het middelste. De oplossingen zullen dan allemaal langzaam uit de gaatjes door de gel heen onzichtbaar naar elkaar toe diffunderen, maar waar een van de bekende antisera een eiwit ontmoet uit het centrale gaatje dat het als antigeen herkent, vormt het juichend stel een witte lijn. Als je dus witte lijnen ziet opkomen tussen het centrale gaatje en de gaatjes van antiserum tegen x en antiserum tegen y, dan weet je dat de onbekende oplossing waarschijnlijk de eiwitten x en y bevatte.
En dan bestaat er nog immuno-elektroforese. Het elektroforeseresultaat, gemaakt zoals we al bespraken, wordt blootgesteld aan een gel waarin een antistof zit. Witte bogen verschijnen dan waar het patroon zijn overeenkomstig antigeen loslaat. Doe al die beschreven methodes bij elkaar, en ik ben er zeker van dat er nieuwe, nog gevoeligere en misschien nog misleidendere uit voort zullen komen.
Maar hoe al die krachten binnen je lichaam gebalanceerd en toch klaar staan, dat is weer iets. Wel kan je een zinvol verhaal maken uit deze hoofdstukken, een novelle waarin eerst een bacterie een lichaam binnenkomt. Het laat wat antigeen los; dat komt bij een plasmacel terecht. Dringt erin door. Cel maakt antistof; laat die vrijkomen; antistof naar bacterie, wordt daar gecombineerd met antigeen, daardoor ook met C'i complement; dat wordt enzym en trekt andere aan, tenslotte ook het lekkerste complement; granulocyt komt aansnellen en eet alles op, sterft; stukje van zijn protoplasma wordt door lymfocyt gevonden en opgegeten; die maakt meer antistof, enzovoort. Dat lijkt allemaal zo vol betekenis, omdat het je leven redt. Het gekke van ons is, dat we het meest ingewikkelde, namelijk je leven, dus het geheel, veel meer als vanzelfsprekend accepteren dan de meer eenvoudige elementen ervan. Zelfs van een witte cel die naar zijn prooi toe kruipt, zeggen we makkelijk: ‘natuurlijk doet hij dat; hij moet toch eten om te leven?’ Wil die cel dat dan, of is hij een willoos deel van een grote samenzwering met als doel: jou in leven te houden?
|
|